将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g);
NH3(g)+HI(g);
②2HI H2(g)+I2(g)
H2(g)+I2(g)
达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则此温度下反应①的平衡常数为
| A.9 | B.16 | C.20 | D.25 |
在常温下发生下列反应:
①16H++10Z-+2XO ="=" 2X2++5Z2+8H2O
="=" 2X2++5Z2+8H2O
②2A2++B2 ="=" 2A3++2B-
③2B-+Z2 ="=" B2+2Z-,根据上述反应,判断下列结论中错误的是( )
| A.溶液中可能发生反应:Z2+2A2+=2A3++2Z- |
| B.Z在①③反应中作还原剂 |
C.氧化性强弱顺序为XO >Z2>B2>A3+ >Z2>B2>A3+ |
D.X2+是XO 的还原产物 的还原产物 |
下列反应的离子方程式书写正确的是( )
| A.钠和冷水反应:Na+2H2O == Na++2OH-+H2↑ |
B.金属铝溶于氢氧化钠溶液:Al+2OH-== AlO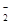 +H2↑ +H2↑ |
| C.金属铝溶于盐酸中:2Al+6H+ == 2Al3++3H2↑ |
| D.铁跟稀硫酸反应:Fe+2H+ == Fe3++H2↑ |
溶液中有0.2mol XO ,加入0.3mol Na2SO3恰好反应,已知Na2SO3被氧化成Na2SO4,则还原产物中X的化合价
,加入0.3mol Na2SO3恰好反应,已知Na2SO3被氧化成Na2SO4,则还原产物中X的化合价
为( )
| A.+4 | B.+3 | C.+1 | D.0 |
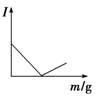
在一定温度下,向不同电解质溶液中加入新物质时,其电流强度(I)随新物质加入量(m)的变化曲线不正确的是( )
| A |
B |
C |
D |
 |
 |
 |
 |
| 向Ba(OH)2溶液中逐滴加入等浓度的H2SO4至过量 |
向醋酸溶液中逐滴加入等浓度的氨水至过量 |
向盐酸溶液中逐滴加入等浓度的NaOH溶液至过量 |
向氨水中逐滴加入等浓度的盐酸至过量 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.标准状况下,22.4 L H2O含有NA个水分子 |
| B.标准状况下,22.4 L空气含有NA个单质分子 |
| C.常温常压下,11.2 L氯气所含的原子数目为NA |
| D.标准状况下,1.12 L O2和1.12 L CO2均含有0.1NA氧原子 |