在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)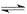 Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
| 温度℃ |
25 |
80 |
230 |
| 平衡常数 |
5×104 |
2 |
1.9×10-5 |
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.25℃时反应Ni(CO)4(g)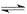 Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
D.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
在8NH3+3Cl2====6NH4Cl+N2反应中,氧化产物与还原产物的分子个数比为( )
| A.8∶3 | B.3∶8 | C.6∶1 | D.1∶6 |
下列离子方程式正确的是( )
A.碳酸氢铵溶液与足量氢氧化钠溶液反应: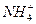 +OH-====NH3·H2O +OH-====NH3·H2O |
| B.Fe(OH)3与氢碘酸溶液混合:Fe(OH)3+3H+====Fe3++3H2O |
| C.电解精炼铜的阴极反应是:Cu2++2e-====Cu |
D.1 mol·L-1的NaAlO2溶液和2.5 mol·L-1的HCl等体积互相均匀混合:2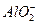 +5H+====Al(OH)3↓+Al3++H2O +5H+====Al(OH)3↓+Al3++H2O |
反应2FeCl3+H2S====2FeCl2+S↓+2HCl改写为离子方程式,正确的是( )
| A.2Fe3++S2-====2Fe2++S↓ | B.Fe3++H2S====Fe2++S↓+2H+ |
| C.2Fe3++H2S====Fe2++S↓+2H+ | D.2FeCl3+S2-====2FeCl2+S↓+2Cl- |
下列各组离子在强酸性无色溶液中共存的是( )
A.Na+K+ Cl- Cl- |
B.Ca2+ Cl- Cl- |
C.K+ Cu2+ Cl- Cl- |
D.Mg2+ Ca2+ Cl-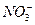 |
与离子方程式Fe3++3OH-====Fe(OH)3↓相对应的化学方程式是( )
| A.FeSO4+2NaOH====Fe(OH)2↓+Na2SO4 |
| B.2Fe(NO3)3+3Mg(OH)2====2Fe(OH)3↓+3Mg(NO3)2 |
| C.Fe2(SO4)3+3Ba(OH)2====2Fe(OH)3↓+3BaSO4↓ |
| D.Fe2(SO4)3+6NaOH====2Fe(OH)3↓+3Na2SO4 |