某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:
A(s)+3B(g) 2C(g)+ D(g);ΔH<0,在一定温度和压强下达到平衡。若平衡时C的物质的量与加入B的物质的量的变化关系如图所示。 则下列说法中正确的是
2C(g)+ D(g);ΔH<0,在一定温度和压强下达到平衡。若平衡时C的物质的量与加入B的物质的量的变化关系如图所示。 则下列说法中正确的是
A若保持压强不变,降低温度时,图中角度a将变小
B若增大压强,缩小容器的体积,平衡向正反应方向移动
C若保持压强不变,再通人B,则再次达到平衡时正、逆反应速率均增大
D平衡时B、C的物质的量之比为1:2
下列说法一定正确的是(NA表示阿伏加德罗常数)
| A.常温下4.4gN2O与标准状况下2.24LCH4均含有0.1NA个分子 |
| B.78g金属钾(K)完全转化为超氧化钾(KO2)时,转移电子数为4NA |
| C.0.1mol/L稀盐酸中,H+数目为0.1NA |
| D.60g二氧化硅晶体中,含S—O键数目为2NA |
下列在指定溶液中的各组离子,能够大量共存的是
| A.使无色酚酞变红的溶液中:S2—、K+、CO32—、C1— |
| B.1mol·L—1的氯化铁溶液中:Na+、C1—、SCN—、Cu2+ |
| C.PH=0的溶液中:S2—、I—、Mg2+、Ba2+ |
| D.水电离的C(H+)=10—13mol·L—1的溶液中:Fe2+、SO42—、K+、NO3— |
容器中发生一个化学反应,反应过程中存在H2O、H2S、S、NH4+、H+、NO3—六种物质。在反应过程中测得NO3—和S的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是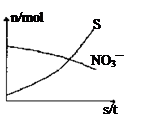
| A.配平后氧化剂与还原剂的化学计量数之比为1:4 |
| B.硫元素在反应中被还原 |
| C.还原剂是含NH4+的物质 |
| D.若生成1molNH4+,则转移电子2mol。 |
下列与有机物结构、性质相关的叙述正确的是
| A.乙醇分子和水分子中都含有羟基,均可与金属钠反应生成氢气 |
| B.苯和乙烯分别与酸性高锰酸钾溶液混合,现象相同 |
| C.淀粉和纤维素均为多糖,属于同分异构体 |
| D.石油的分馏、煤的干馏、煤的气化和液化均为物理变化 |
下列说法不正确的是
A.在固定体积的密闭容器中发生可逆反应A(s)+B(g)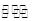 C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态 C(g)+D(g),当混合气体的密度不再改变时,说明已达到化学平衡状态 |
B.对于反应C(s)+CO2(g)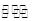 2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大 2CO(g)△H>0,改变某一条件,若化学平衡常数增大,则反应速率也一定增大 |
C.向0.1mol·L-1的NH3·H2O中加入氯化铵固体,则溶液中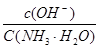 增大 增大 |
D.常温下向Mg(OH)2悬浊液中加入MgCl2浓溶液后,溶液中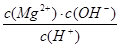 不变 不变 |