常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0. 1mol·L-1NaOH 溶液: K+、Na+、SO42- 、CO32- |
| B.0. 1mol·L-1Na2CO3溶液:K+、Ba2+、NO3- 、Cl- |
| C.0. 1mol·L-1FeCl3溶液:K+、NH4+、I-、SCN- |
| D.c(H+)/c(OH-)= 1×1014的溶液:Ca2+、Na+、ClO-、NO3- |
现有如下几个离子方程式①CaCO3+2H+===Ca2++H2O+CO2↑
② 
③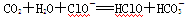
④ ,
,
由此得出的如下结论中不正确的是
A.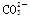 与H+、Ca2+不能大量共存 与H+、Ca2+不能大量共存 |
| B.H2CO3的酸性比HClO强,比H2SO3弱 |
| C.H2SO3是一种强酸 |
| D.H2CO3、HClO都属于弱酸 |
下列溶液一定呈中性的是
| A.c(H+)=c(OH-)=10-6 mol·L-1的溶液 |
| B.pH=7的溶液 |
| C.滴入酚酞显无色的溶液 |
| D.酸与碱恰好完全反应生成正盐的溶液 |
短周期主族元素A,B,C,D,E的原子序数依次增大,其中只有C为金属元素,B是地壳中含量最多的元素,C原子的最外层电子数和A相等;C,D两元素原子的质子数之和是A,B两元素质子数之和的3倍,下列叙述正确的是
A.元素的原子半径:A<B<C<D<E
B.对应氢化物的热稳定性:D>E
C.B与C、B与D形成的化合物中化学键类型相同
D.5种元素中最高价氧化物对应的水化物酸性最强的是E
下列有关说法中不正确的是
| A.铁与Cl2、盐酸均能发生反应,但生成的含铁物质组成不同 |
| B.分别加热蒸干并灼烧铁、铝的氯化物溶液,最后得到的物质均为金属氧化物 |
| C.等物质的量的Na、Cu、Al与足量氯气反应时,消耗的氯气一样多 |
| D.常温下,铁片、铝片与浓硫酸的反应均只能停留在金属的表面上 |
下列关于Na2O2的叙述正确的是
| A.Na2O2晶体中的阴离子与阳离子的物质的量之比为1∶1 |
| B.Na2O2晶体为离子晶体,且含极性共价键 |
| C.Na2O2应保存于带玻璃塞的广口瓶中 |
| D.Na2O2与盐酸反应,不仅有盐和水生成,同时会放出无色气体 |