已知298K时,2SO2(g)+O2(g) 2SO3(g);△H=-197kJ·mol-1。现有同一温度下的三个体积相同的密闭容器,在第一个容器中通入2molSO2和1molO2,达到平衡时,反应放出的热量为Q1;向第二个密闭容器中通入1molSO2和0.5molO2,达到平衡时放出的热量为Q2;在第三个密闭容器中通入1molSO2、0.5molO2和1molSO3达到平衡时放出的热量为Q3。下列关系正确的是
2SO3(g);△H=-197kJ·mol-1。现有同一温度下的三个体积相同的密闭容器,在第一个容器中通入2molSO2和1molO2,达到平衡时,反应放出的热量为Q1;向第二个密闭容器中通入1molSO2和0.5molO2,达到平衡时放出的热量为Q2;在第三个密闭容器中通入1molSO2、0.5molO2和1molSO3达到平衡时放出的热量为Q3。下列关系正确的是
| A.Q1=Q3=197kJ | B.Q1=Q3<197kJ |
| C.Q1=2Q2 <197kJ | D.Q2<Q1<197kJ |
室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是( )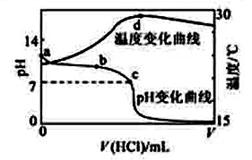
| A.a点由水电离出的c(H+)=1.0×10-14mol/L |
| B.b点:c(NH4+)+c(NH3·H2O) > c(Cl-) |
| C.c点:反应消耗的HCl 和NH3·H2O 的关系为:n(HCl)= n(NH3·H2O) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
向盛有一定量氢氧化钠溶液的烧杯中通入标准状况下448mL氮气和二氧化碳的混合气体后得到溶液A,在溶液A中逐滴加入0.1 mol/L的稀盐酸至过量,并将溶液加热,产生的二氧化碳气体的物质的量与加入稀盐酸的体积的关系如图所示(忽略二氧化碳的溶解和氯化氢的挥发)。下列说法正确的是()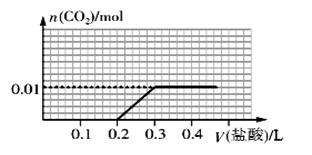
| A.原混合气体中氮气与二氧化碳体积之比为1∶4 |
| B.在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为CO32-+H-==HCO3- |
| C.溶 液 A 中 含 有 0 . 01 mol NaOH 和0.01 mol Na2CO3 |
| D.当加入0.1 L稀盐酸时,此时溶液中离子浓度大小关系为c(Na+)>c(Cl-)=c(CO32-)>c(OH-)>c(H+) |
由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种或两种以上元素,它们分子中质子总数均与氩原子的质子数相同,已知甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是()
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第2周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲含有某相同元素,且该元素在二者中的百分含量相同,则丁中一定含有-l价元素 |
某化学研究性学习小组对电解质溶液作如下的归纳总结(均在常温下),其中正确的是()
①常温下,pH=1的强酸溶液,加水稀释后,溶液中各离子浓度一定都降低
②pH=2的盐酸和pH=1的盐酸, 之比为2:1
之比为2:1
③pH相等的四种溶液:a.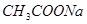 ;b.
;b.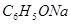 ;c.
;c.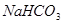 ;d.
;d.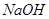 。其溶液物质的量浓度由小到大顺序为d、b、c、a
。其溶液物质的量浓度由小到大顺序为d、b、c、a
④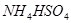 溶液中滴加NaOH溶液至溶液pH=7,则
溶液中滴加NaOH溶液至溶液pH=7,则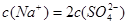
⑤已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw;则三者关系为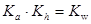
⑥甲、乙两溶液都是强电解质,已知甲溶液的pH是乙溶液pH的两倍,则甲、乙两溶液等体积混合,混合液pH可能等于7
| A.③⑤⑥ | B.③④⑥ | C.④⑤⑥ | D.①②④ |
当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
| A.当电池负极消耗m g气体时,电解池阳极同时有m g气体生成 |
| B.电池的负极反应式为:O2+2H2O+4e-=4OH- |
| C.电解后c(Na2CO3)不变,且溶液中有晶体析出 |
| D.燃料电池中c(KOH)不变;电解池中溶液pH变大 |