下列有关说法正确的是
| A.放热反应在任何条件都能自发进行 |
| B.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液 |
| D.电解精炼铜时,外电路中转移电子数为2NA个时,阳极铜质量减少64g |
某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为
A. |
B.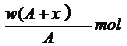 |
C.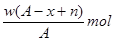 |
D. |
下列事实,不能说明氯元素的非金属性比硫元素强的是
| A.氯气比硫单质更易与氢气反应 | B.HClO4酸性比H2SO4强 |
| C.盐酸是强酸,氢硫酸是弱酸 | D.受热时,氯化氢比硫化氢稳定 |
从化学键的角度看化学反应的实质是“旧化学键的断裂,新化学键的形成”,下列既有旧化学键的断裂,又有新化学键的形成的变化是
| A.酒精溶解于水 |
| B.使石墨转变为金刚石 |
| C.氯化钠受热熔化 |
| D.NaOH作为干燥剂吸水 |
下列各分子中,所有原子都满足最外层为8电子结构的是
| A.H2O | B.BF3 | C.CCl4 | D.PCl5 |
关于离子键、共价键的各种叙述中,下列说法中正确的是
| A.在离子化合物里,只存在离子键,没有共价键 |
| B.非极性键只存在于双原子的单质分子(如Cl2)中 |
| C.在共价化合物分子内,一定不存在离子键 |
| D.由不同元素组成的多原子分子里,一定只存在极性键 |