下列有关实验操作、现象和解释或结论都正确的是
| 选项 |
操作 |
现象 |
解释或结论 |
| A |
过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 |
溶液呈红色 |
稀HNO3将Fe氧化为Fe3+ |
| B |
Al箔插入稀HNO3中 |
无现象 |
Al箔表面被稀HNO3氧化, 形成致密的氧化膜 |
| C |
向某溶液中滴加稀NaOH溶液,将湿润 红色石蕊试纸置于试管口 |
试纸未变蓝 |
不能确定该溶液中是否含 有NH4+ |
| D |
向紫色石蕊试液中通入SO2 |
溶液褪色 |
SO2有漂白性 |
等物质的量的Na2CO3和NaHCO3分别与足量的同浓度盐酸溶液充分反应,其中
| A.Na2CO3放出的CO2多 | B.NaHCO3放出的CO2多 |
| C.Na2CO3放出CO2的速度快 | D.NaHCO3放出CO2的速度快 |
下列区分Fe(OH)3悬浊液和Fe(OH)3胶体的方法中,正确的是
| A.静置片刻出现分层现象的是Fe(OH)3胶体 |
| B.用放大镜观察,颗粒大小为1~100nm的是Fe(OH)3胶体 |
| C.用光束照射,能产生丁达尔现象的是Fe(OH)3胶体 |
| D.看颜色,有色的是Fe(OH)3胶体 |
据报道,一科学小组由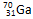 和
和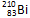 两原子经核聚合,并放出一定数目的中子而制得质量数为275,质子数为114的某原子。则两原子在核聚合过程中放出的中子数目是
两原子经核聚合,并放出一定数目的中子而制得质量数为275,质子数为114的某原子。则两原子在核聚合过程中放出的中子数目是
| A.161 | B.5 | C.166 | D.52 |
熔融烧碱样品应使用下列哪种器皿
| A.石英坩埚 | B.氧化铝耐高温坩埚 | C.生铁坩埚 | D.瓷坩埚 |
下列有关试剂的保存方法,错误的是
| A.碘保存在棕色细口玻璃试剂瓶中 |
| B.少量的钠保存在煤油中 |
| C.新制的氯水通常保存在棕色细口玻璃试剂瓶中 |
| D.氢氧化钠溶液用带橡胶塞的试剂瓶贮存 |