下列离子方程式正确的是
| A.NO2通入AgNO3溶液中:3NO2+H2O=2NO3-+NO+2H+ |
| B.过量的SO2通入NaOH溶液中:SO2+2OH-=SO32-+H2O |
| C.过量NaOH滴入NH4HCO3稀溶液中:NH4++OH-=NH3·H2O |
| D.铜片加入稀HNO3中:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O |
常温下,下列各组离子在给定条件下一定能大量共存的是()
| A.pH=1的溶液中:K+、Na+、S2-、SO32- |
| B.加入铝粉可以放出氢气的溶液中:Mg2+、K+、NO3-、Cl- |
| C.透明的溶液中:Cu2+、H+、Cl-、SO42- |
| D.含有Fe3+的溶液中:K+、H+、I-、Cl- |
设NA为阿伏加德罗常数的值,下列说法中正确的是()
| A.18g重水(D2O)中含有的电子数为10NA |
| B.1mol钠加热时与O2反应失去的电子数为NA |
| C.1L0.1mol/L的盐酸中,含有的HCl分子数为NA |
| D.在标准状况下, 相同物质的量的SO2和SO3的体积相同 |
将淀粉与氯化钾混合液装在半透膜中,浸泡在装有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是()
| A.加入碘水变蓝色 | B.加入硝酸银溶液不产生白色沉淀 |
| C.加入硝酸银溶液产生白色沉淀 | D.加入碘水不变色 |
下列叙述正确的是()
| A.SO2的水溶液能够导电,但SO2是非电解质 |
| B.饱和氯水的导电性很好,所以氯气是强电解质 |
C. 和 和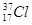 为不同的核素,二者核外电子数不同 为不同的核素,二者核外电子数不同 |
| D.化合反应和分解反应一定属于氧化还原反应 |
下列说法正确的是()
| A.能与酸反应的氧化物,一定是碱性氧化物 |
| B.Li、Na、K的密度逐渐增大 |
| C.Cl2、Br2、I2中,由于分子间作用力逐渐越大,所以分子越来越稳定 |
| D.物质溶于水时,有些化学键被破坏,有些化学键不被破坏 |