Ⅰ.已知在常温常压下:
① 2CH3OH(l)十3O2(g)=2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l)=H2O(g) △H="+" 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
Ⅱ.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如下图:

(1)在Na3PO4溶液中,c(Na+)/c(PO43-) 3(填“>”“=”“<”),向Na3PO4溶液中滴入稀盐酸后 ,pH从10降低到5的过程中发生的主要反应的离子方程式为 。
(2)从图中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是 。(填选项字母)
A、C(Na+)> C(H2PO4 -)> C(H+)> C(HPO4 2-)> C(H3PO4 )
B、C(Na+)> C(H2PO4 -)> C(OH-)> C( H3PO4)> C(HPO4 2- )
C、C(H+)+ C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-)+C(H3PO4 )
D、C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4 )
(3)假设25℃条件下测得0.1 mol·L–1的Na3PO4溶液的pH=12 ,近似计算出Na3PO4的第一步水解的水解常数Kh(写出计算过程,忽略Na3PO4的第二、第三步水解,结果保留两位有效数字)。
Ⅲ.化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染。电化学降解NO3-的原理如图所示。电源正极为 (填A或B),阴极反应式为 。
下列电离方程式错误的是()
A.Ba(OH)2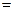 Ba2+ +2OH- Ba2+ +2OH- |
B.NaHSO4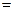 Na+ +H+ +SO42- Na+ +H+ +SO42- |
C.MgC l2 l2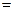 Mg2+ +2Cl- Mg2+ +2Cl- |
D.NaHCO3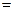 Na+ +H+ +CO32- Na+ +H+ +CO32- |
下列说法正确的是()
| A.可用丁达尔现象区分溶液与胶体 |
| B.生石灰与水混合的过程只发生物理变化 |
| C.胶体是一种纯净物 |
| D.CuSO4·5H2O是一种混合物 |
常温下,Ksp(CaSO4)=9´10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是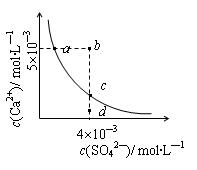
| A.在任何溶液中,c(Ca2+)、c(SO42-)均相等 |
B.b点将有沉淀生成,平衡后 溶液中c(SO42-)一定等于3´10-3 mol·L—1 溶液中c(SO42-)一定等于3´10-3 mol·L—1 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.d点溶液通过蒸发可以变到c点 |
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备
高纯度的镍,下列叙述 正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
| A.阳极发生还原反应,其电极反应式:Ni2++2e-→Ni |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu和Pt |
用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、N a+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是 ( )
a+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是 ( )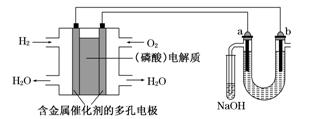
| A.电池工作时,正极反应式为:O2+2H2O+4e-→4OH- |
| B.电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 |
| C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 |
| D.忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2 |