下列叙述或表示方法正确的是( )
| A.Na2O2是离子化合物,其阴、阳离子个数比为1∶1 |
B.N(NO2)3(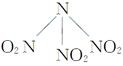 )既有氧化性又有还原性 )既有氧化性又有还原性 |
C.NH4HCO3溶液与过量的NaOH溶液微热反应:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.铜片溶于稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
下列常见现象与胶体无关的是()
| A.清晨在密林中看到一缕缕的光束 |
| B.向豆浆中加入硫酸钙使蛋白质等聚沉,制成可口的豆腐 |
| C.FeCl3溶液加入NaOH溶液产生红褐色沉淀 |
| D.利用电泳将油漆、乳胶、橡胶等微粒均匀地沉积在镀件上 |
相等物质的量的H2O和H2O2相比较,下列有关叙述中正确的是()
①它们所含的分子数目之比为1∶1
②它们所含的原子总数目之比为3∶4
③它们所含的O原子数目之比为1∶2
④它们所含的H原子数目之比为1∶1
⑤它们所含的质子数目之比为5∶9
| A.①②③ | B.③④⑤ | C.①②④ | D.①②③④⑤ |
下列反应完成后有沉淀生成的是()
| A.BaCl2溶液与Na2CO3溶液加足量CH3COOH溶液 |
| B.Ba(OH)2溶液与KNO3溶液加足量稀硫酸 |
| C.AgNO3溶液与Na2CO3溶液加足量稀硝酸 |
| D.Ca(OH)2溶液与FeCl3溶液加足量稀硝酸 |
实验室制取氧气的反应为2KClO3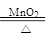 2KCl+3O2↑,反应后从剩余物中回收纯净的二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体) ()
2KCl+3O2↑,反应后从剩余物中回收纯净的二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体) ()
| A.溶解、过滤、蒸发、洗涤 | B.溶解、过滤、洗涤、干燥 |
| C.溶解、蒸发、洗涤、过滤 | D.溶解、洗涤、过滤、加热 |
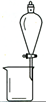
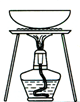
完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是()
| A.用CCl4提取溴水中的Br2 |
B.从KI和I2的固体混合物中回收I2 |
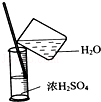
C.稀释浓硫酸 |
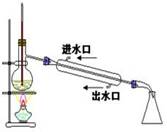
D.工业酒精制备无水酒精 |
 |
 |
 |
 |