铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是
| A.铊是易导电的银白色金属 | B.能生成+3价离子化合物 |
| C.T1(OH)3是两性氢氧化物 | D.Tl的失电子能力比Al强 |
已知一定温度下,有下列难溶电解质的溶解平衡数据:
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| Ksp/25 ℃ |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
| 完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3~4 |
则对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是( )。
A.向该混合溶液中加过量铁粉,能观察到红色固体析出
B.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C.该混合溶液中c(SO42-)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
D.向该混合溶液中加入适量氯水,并调节pH至3~4后过滤,能得到纯净的CuSO4溶液
下列实验操作中,主要不是从安全因素考虑的是( )。
A.用NH4Cl、Ca(OH)2制备NH3时,可用如图所示装置吸收尾气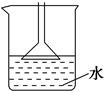 |
| B.制备Fe(OH)2时,吸有NaOH溶液的胶头滴管要插入亚铁盐溶液中再挤出NaOH溶液 |
| C.加热试管中的固体时,试管口应略向下倾斜 |
| D.用氢气还原氧化铜时,先通一会氢气,再加热氧化铜 |
下列与化学反应能量变化相关的叙述正确的是( )。
| A.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| B.1 mol S完全燃烧放热297.3 kJ,其热化学方程式:S+O2=SO2 ΔH=-297.3 kJ·mol-1 |
| C.1 mol H2SO4与1 mol Ba(OH)2反应生成1 mol BaSO4沉淀时放出的热量叫做中和热 |
| D.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
某化学学习小组学习电化学后,设计了下面的实验装置图:
下列有关该装置图的说法中正确的是( )。
| A.合上电键后,盐桥中的阳离子向甲池移动 |
| B.合上电键后,丙池为电镀银的电镀池 |
| C.合上电键后一段时间,丙池中溶液的pH增大 |
| D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体 |
下列表示对应化学反应的离子方程式正确的是( )。
| A.向AlCl3溶液中加入过量浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
| B.将含有0.1 mol Ba(OH)2的溶液与含有0.2 mol NaHSO4的溶液混合:H++SO42-+OH-+Ba2+=BaSO4↓+H2O |
| C.向澄清石灰水中通入过量CO2:OH-+CO2=HCO3- |
| D.Na2O2溶于水:2O2-+2H2O=4OH-+O2↑ |