微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为: Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-,根据上述反应式,判断下列叙述中正确的是
| A.在使用过程中,电池负极区溶液的pH减小 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
在测定中和反应反应热的实验中,下列叙述错误的是
| A.向量热计中加入盐酸,搅拌后的温度为初始温度 |
| B.实验中可使酸或碱略过量 |
| C.向量热计中加碱液时,碱液的温度应与酸的温度相同 |
| D.可以用氢氧化钾代替氢氧化钠,浓硫酸代替盐酸 |
右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊溶液。下列实验现象中错误的是
| A.a电极附近呈蓝色,b电极附近呈红色 |
| B.a电极附近呈红色,b电极附近呈蓝色 |
| C.逸出气体的体积,a电极的大于b电极的 |
| D.a、b两电极都逸出无色无味气体 |
下列说法正确的是
| A.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H相同 |
| B.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 |
| C.已知:①2H2(g) +O2(g) =2H2O(g) △H="-a" kJ·mol-1, ②2H2(g)+O2 (g)= 2H2O(1) △H="-b" kJ·mol-1,则a>b |
| D.已知:①C(s,石墨)+O2 (g)=CO2(g) △H="-" 393.5kJ·mol-1, |
②C(s,金刚石)+O2(g)=CO2 (g) △H="-" 395.0 kJ·mol-1
则C(s,石墨)=C(s,金刚石) △H=" -1.5" kJ·mol-1
关于下列各装置图的叙述中,不正确的是: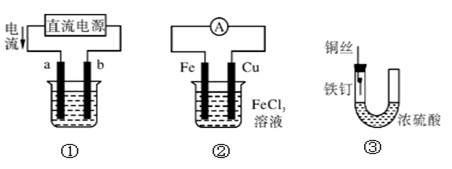
| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.用装置①进行电镀,镀件接在b极上 |
| C.装置②的总反应是:Cu+2Fe3+===Cu2++2Fe2+ |
| D.装置③中的铁钉几乎没被腐蚀 |
下列有关叙述错误的是
| A.化学反应均伴随着能量的变化 |
| B.需要加热才能发生的反应不一定是吸热反应 |
| C.物质的化学能可以在一定条件下转化为热能、电能为人类利用 |
| D.吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值 |