根据表中信息,判断下列叙述中正确的是
| 序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
|
FeBr2 |
/ |
|
Cl- |
| ② |
MnO2 |
浓盐酸 |
/ |
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:MnO2>Fe3+>Cl2>Br2
C.表中②组反应的氧化产物是MnCl2,1molMnO2电子转移数目是2NA
D.表中③组反应的离子方程式为:2MnO4—+3H2O2+6H+=2Mn2++4O2↑+6H2O
以下实验能获得成功的是
| A.用酸性KMnO4溶液鉴别乙烯和乙炔 |
| B.将铁屑、溴水、苯混合制溴苯 |
| C.在苯酚溶液中滴入少量稀溴水出现白色沉淀 |
| D.将铜丝的酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
下列说法中正确的是()
| A.汽油、柴油和植物油都是碳氢化合物 |
| B.利用核磁共振氢谱图可鉴别1-溴丙烷和2-溴丙烷 |
| C.甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
| D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键 |
聚合硫酸铁可用于水的净化,化学式可表示为[Fea(OH)b(SO4)c]m,取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份,一份溶液加入足量的BaCl2溶液,得到白色沉淀BaSO44.66g。另一份溶液,加入足量的NaOH溶液后过滤对滤出固体洗涤,后灼烧得到红棕色固体Fe2O3质量为1.6g,该聚合硫酸铁样品中a:b的比值是(已知:BaSO4的相对原子质量为233 ,Fe2O3相对原子质量为160)
| A.1:1 | B.2:1 | C.3:1 | D.2:5 |
用氯气给自来水消毒时通常要发生化学变化,其变化的微观过程如下图表示则下列有关的分析判断正确的是
| A.反应物中无单质 | B.反应前后元素种类不变 |
| C.该反应类型属于置换反应 | D.该反应类型属于复分解反应 |
如图为甲、乙两种固体物质在水中的溶解度曲线,下列说法错误的是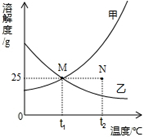
| A.甲物质的溶解度随温度的升高而增大 |
| B.在t1℃时,M点表示甲、乙两物质的溶解度相等 |
| C.在t2℃时,N点表示甲物质的不饱和溶液 |
| D.在t1℃时,100g乙物质的饱和溶液中溶质的质量是25g |