某微粒的结构示意图为 , 试回答:
, 试回答:
(1)当x-y=10时,该粒子为 (选填“原子”或“阳离子”、“阴离子”)。
(2)当y=8时,该粒子可能是(用化学式表示,任填3种) 、 、 。
(3)请写出实验室制取y=7时元素对应单质的离子方程式: 。
下图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。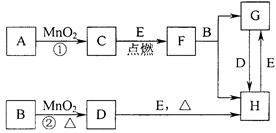
(1)写出有关物质的名称或化学式:F,H。
若反应①是在加热条件下进行,则A是;若反应①是在常温条件下进行,则A是。
(2)写出B与MnO2共热获得D的离子方程式 。
。
(3 )B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4
)B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4 mo1/L
mo1/L  ,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象,沉淀能够发生转化的原因是。
,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象,沉淀能够发生转化的原因是。
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)Z原子的结构示意图为
(2)用电子式表示X与W组成的化合物的形成过程
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为 。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下A与NaOH溶液反应的离子方程式 。
。
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式 。
。
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+________→________+________+________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1mol氧化剂_______(填“得到”或“失去”)________mol电子。
下图是煤化工产业链的一部分,试运用所学知识,解决下列问题: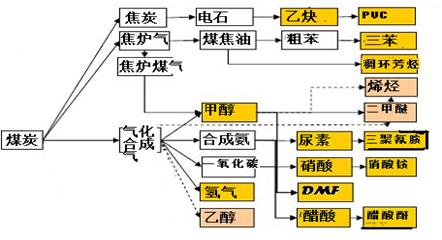
(1)该产业链中合成氨的反应在较低温下能否自发进行?。
(2)已知该产业链中某反应的平衡表达式为:
它所对应的化学反应为:。
(3)已知在一定温度下,各反应的平衡常数如下:
C(s)+CO2(g) 2CO(g),K1
2CO(g),K1
CO(g)+H2O(g  H2(g)+CO2(g),K2
H2(g)+CO2(g),K2
C(s)+H2O(g) CO(g)+H2(g),K3
CO(g)+H2(g),K3
则K1、K2、K3之间的关系是:。
(4)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)  H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
该反应的正反应方向是反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为:。
(5)从图中看出氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如NO、NO2、N2O4等。已知NO2和N2O4的结构式分别是 和
和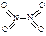 。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为。
。已知N-N键键能为167kJ·mol-1,NO2中氮氧键的键能为466kJ·mol-1,N2O4中氮氧键的键能为438.5kJ·mol-1。请写出NO2转化为N2O4的热化学方程式为。
对反应N2O4(g)  2NO2(g),在温度为T1
2NO2(g),在温度为T1 、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。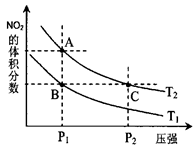
下列说法正确的是 。
A.A、C两 点的反应速率:A>C
点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
(6)以上述产业链中甲醇为燃料制成燃料电池,请写出在氢氧化钾介质中该电池的负极反应式。
[化学—选修5:有机化学基础]
G是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
(1)化合物G的分子式为。B转化为C的反应所属反应类型为。
(2)化合物D的名称为,它的核磁共振氢谱应有组不同类型的峰,它与碳酸氢钠溶液反应的化学方程式为。
(3)化合物E的同分异构体中,能够使三氯化铁溶液显紫色,且能 够水解生成化合物B的有种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为。
够水解生成化合物B的有种。这其中核磁共振氢谱图有四组不同类型峰的同分异构体的结构简式为。
(4)请分别写出A→B、D→E两个转化过程中的反应方程式:、。