设NA是阿伏加德罗常数的值,下列说法正确的是
| A.1 L1mol·L-1的NaClO溶液中含有ClO-的数目为NA |
| B.60g二氧化硅含有的共价键数为2NA |
| C.7.8g钾与100mL 1mol·L-1盐酸充分反应生成气体分子数为0.1NA |
| D.标准状况下,7.1g 氯气与足量的石灰乳充分反应,转移电子数为0.2NA |
下列物质中,碳的质量分数相同的是
| A.CH4、C2H6 | B.HCHO、C6H12O6 |
| C.CH3CH2OH、CH3COOH | D.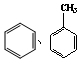 |
有机物分子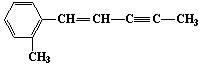 中最多有多
中最多有多 少个原子共面
少个原子共面
| A.12 | B.16 | C.20 | D.24 |
下列物质的碳碳键长大小关系为①乙烷②乙烯③乙炔④苯
| A.①>②>③>④ | B.④>③>②>① | C.①>④>②>③ | D.④>①>②>③ |
某烃的结构简式为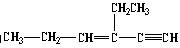 ,分子中含有四面体结构的碳原子数为a,
,分子中含有四面体结构的碳原子数为a, 在同一条直线上的碳原子数最多为b,一定在
在同一条直线上的碳原子数最多为b,一定在 同一平面内的碳原子数为c,则a、b、c分别是
同一平面内的碳原子数为c,则a、b、c分别是
| A.4、3、5 | B.2、5、4 | C.4、3、6 | D.4、6、4 |
下列关于有机化学发展史的说法错误的是网]
| A.中国科学家成功合成了结晶牛胰岛素,标志着人类合成蛋白质时代的开始 |
| B.德国化学家李比希提出运用同位素示踪法研究化学反应历程 |
| C.瑞典科学家贝采利乌斯提出有机化学的概念,使之成为化学的一个重要分支 |
| D.德国化学家维勒用氰酸铵合成尿素,从而打破了无机物和有机物的界限 |