下列关于硫酸工业生产过程的叙述错误的是
| A.在接触室中使用铁粉作催化剂 |
| B.在接触室中运用热交换技术可充分利用能源 |
| C.把硫铁磨成细粉末,可以提高原料的利用率 |
| D.该反应采用450~500℃主要是因为该温度下催化剂活性好 |
下列说法中正确的是
| A.C60气化和I2升华克服的作用力相同 |
| B.甲酸甲酯和乙酸的分子式相同,它们的熔点相近 |
| C.氯化钠和氯化氢溶于水时,破坏的化学键都是离子键 |
| D.用作高温高硬度结构陶瓷材料的Si3N4固体是分子晶体 |
X、Y、Z均为短周期元素,其简单离子X+、Y3+、Z2-的核外电子层结构相同。下列说法不正确的是
| A.原子序数:Y>X>Z | B.碱性:XOH>Y(OH)3 |
| C.单质的还原性:X>Y | D.离子半径:X+>Y3+>Z2- |
第3周期元素的原子,其最外层p能级上仅有一个未成对电子,它最高价氧化物对应的水化物的酸根离子可能是
| A.RO2- | B.RO3- | C.RO42- | D.RO4- |
下列数据是对应物质的熔点,结合所学知识,有关的判断错误的是
| Na2O |
Na |
AlF3 |
AlCl3 |
Al2O3 |
BCl3 |
CO2 |
SiO2 |
| 920 ℃ |
97.8 ℃ |
1291 ℃ |
190 ℃ |
2073 ℃ |
-107 ℃ |
-57 ℃ |
1 723 ℃ |
A.只要含有金属阳离子的晶体就一定是离子晶体
B.在共价化合物分子中各原子都形成8电子稳定结构
C.同族元素的氧化物可形成不同类型的晶体
D.金属晶体的熔点不一定比分子晶体的高
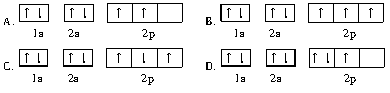
下列轨道表示式能表示氮原子的最低能量状态的是