处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。
已知:CO(g)+ 1/2 O2(g)  CO2(g) ∆H=-283.0 kJ/mol
CO2(g) ∆H=-283.0 kJ/mol
S(g)+ O2(g) SO2(g) ∆H=-296.0 kJ/mol
SO2(g) ∆H=-296.0 kJ/mol
下列说法不正确的是:
| A.两个反应均为氧化还原反应 |
| B.CO2与SO2可以用澄清石灰水鉴别 |
| C.CO2分子中各原子最外层均为8电子稳定结构 |
D.相同条件下:2CO(g)+SO2(g)  S(g)+2CO2 (g)∆H=-270kJ/mol S(g)+2CO2 (g)∆H=-270kJ/mol |
下列叙述不正确的是
A.苯、乙醇和乙酸都能发生取代反应  |
B.等物质的量的乙醇和乙酸完全燃烧时所需氧气的质量相等 |
C.乙醇、乙酸和乙酸乙酯能用饱和NaHCO3溶液鉴别 |
D.乙烷和丙烯的物质的量各1mol,完成燃烧生成3molH2O |
将等体积的苯、汽油和水在试管中充分混合后静置。下图示现象正确的是 
下列有关化学用语使用正确的是
| A.乙烯的结构简式为:CH2CH2 |
| B.CaC2的电子式为:Ca2+ |
C.原子核内有8个中子的氧原子:  O O |
D.对氯甲苯的结构简式: |
标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断中正确的是
| A.反应完成后,O2剩余 |
| B.原混合气体中,C2H4和C2H2的体积共为1.9L |
| C.反应完全后,生成水的质量为9g |
| D.原混合气体中,CO与CH4的体积比一定为1:1 |
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面)。有关该有机物分子的说法不正确的是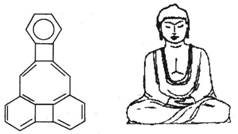
A.属于芳香烃 B.属于苯的同系物
C.分子中含有22个碳原子 D.一氯代物只有3种