相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:
X2 (g+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热46.3 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>0) |
下列叙述不正确的是
A.容器①中达到平衡时,Y2的转化率为50%
B.Q="27.78" kJ
C.若容器①体积改为1.0 L.则达平衡时放出的热量大于46.3 kJ
D.容器①、②中反应的平衡常数相等,K=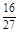
下列溶液一定呈碱性的是
| A.溶液中c(OH-)>c(H+) | B.溶液中含有OH‑离子 |
| C.滴加甲基橙后溶液显红色 | D.滴加甲基橙后溶液显黄色 |
下列说法不正确的是
| A.在化学反应进行的过程中放出或吸收的热量称为反应热。 |
| B.在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热。 |
| C.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量。 |
| D.在101Kpa时,1mol物质完全燃烧生成稳定氧化物时,所放出的热量叫做该物质的燃烧热。 |
在298K、100kPa时,已知:2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g)ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)ΔH3
则⊿H3与⊿H1和⊿H2间的关系正确的是
| A.⊿H3=⊿H1+2⊿H2 | B.⊿H3=⊿H1+⊿H2 |
| C.⊿H3=⊿H1-2⊿H2 | D.⊿H3=⊿H1-⊿H2 |
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
| A.υ(W)=3υ(Z) | B.2υ(X)=3υ(Z) | C.2υ(X)=υ(Y) | D.3υ(W)=2υ(X) |
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH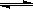 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
| A.加入少量NaOH固体,平衡向逆反应方向移动 |
| B.升高温度,平衡向正反应方向移动 |
| C.加入水稀释,溶液中c(H+)一定增大 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |