向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g) SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是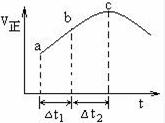
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.△t1=△t2时,SO2的转化率:a~b段小于b~c段 |
高温下,某反应达平衡,平衡常数 恒容时,温度升高H2浓度减小。下列说法正确的是()
恒容时,温度升高H2浓度减小。下列说法正确的是()
| A.该反应化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) |
B.恒温恒容下,增大压强 ,H2浓度一定减小 ,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
| D.该反应的焓变为正值 |
工业上常用氨碱法制取纯碱,是将氨和二氧化碳先后通 入饱和食盐水而析出小苏打,再经过滤,焙烧而得纯碱。但不能用氨碱法制取
入饱和食盐水而析出小苏打,再经过滤,焙烧而得纯碱。但不能用氨碱法制取 碳酸钾,原因可能是 ( )
碳酸钾,原因可能是 ( )
| A.KHCO3溶解度较大 | B.KHCO3溶解度较小 |
| C.K2CO3溶解度较小 | D.K2CO3溶解度较大 |
下列各组离子在指定溶液中能大量共存的是()
①无色溶液中:K+、Cu2+、Na+、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
③加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、NH4+
④由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、I-
⑤使pH试纸变为蓝色的溶液:Na+、C1-、S2-、ClO-⑥无色溶液中:K+、Al3+、NO3-、HCO3-
| A.①②⑤ | B.③⑤⑥ | C.②④ | D.②④⑥ |
设NA表示阿伏加德罗常数的值,下列说法正确的是 ()
()
| A.2.4g镁在二氧化碳中燃烧所转移的电子总数为0.2NA |
| B.7.1g Cl2与足量NaOH(aq)反应时转移的电子总数为0.2 NA |
| C.1 L1 mol/L的Na2CO3(aq)中CO32-与HCO3-的离子数之和为NA |
| D.1 mol NaHSO4晶体中离子总数为3NA |
下列 离子方程式正确的是
离子方程式正确的是
()
A.硫化钠的水解反应:S2-+H3O+ HS-+H2O HS-+H2O |
| B.在氯化亚铁溶液中加入稀硝酸:3Fe2+ + 4H+ + NO3-=3Fe3+ + NO↑ + 2H2O |
| C.向Ca(HCO3)2溶液中加入足量的氢氧化钠溶液: Ca2++HCO3-+OH-=CaCO3↓ + H2O |
D.用铜为电极电解稀硫酸溶液: 2H2O  O2↑ + 2H2 ↑ O2↑ + 2H2 ↑ |