电化学在日常生活中用途广泛,图甲是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2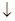 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是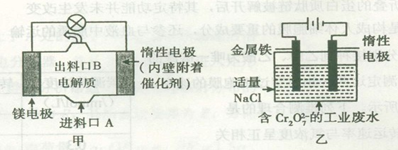
A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2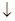 |
| B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| C.图乙电解池中,若有0.084 g阳极材料参与反应,则阴极会有336 mL的气体产生 |
| D.若图甲燃料电池消耗3.6 g镁产生的电量用以图乙废水处理,理论上可产生10.7 g氢氧化铁沉淀 |
已知1 mol红磷 转化为1 mol白磷,吸收18.39 kJ热量.
转化为1 mol白磷,吸收18.39 kJ热量.
4P(红,s)+5O2(g)===2P2O5(s) ΔH1
4P(白,s)+5O2(g)===2P2O5(s) ΔH2
则ΔH1与ΔH2的关系正确的是()
| A.ΔH1=ΔH2 | B.ΔH1>ΔH2 | C.ΔH1<ΔH2 | D.无法确定 |
逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是( )
| A.单质都是由同种元素组成的,只含一种元素的物质一定是纯净物 |
| B.金属铝排在金属活动性顺序表中氢元素的前面,铝与酸反应一定放出氢气 |
| C.中和反应都有盐和水生成,有盐和水生成的反应都属于中和反应 |
| D.氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物 |
根据下图海水综合利用的工业流程图,判断下列说法正确的是( )
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br-需消耗2. 24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
下列关系不正确的是()
| A.离子半径:Cl->F->Na+>Al3+ | B.熔点:石英>食盐>冰>干冰 |
C.结合氢离子的能力:SO42->SO32->CO32 - - |
D.热稳定性:PH3<H2S<HCl<HF |
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。则甲和X不可能是()
| A.甲为C和X为O2 | B.甲为SO2和X为NaOH溶液 |
| C.甲为Fe和X为Cl2 | D.甲为AlCl3溶液和X为NaOH溶液 |