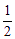(2014届江西省九江市七校高三第二次联考化学试卷)
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。下图为RFC工作原理示意图,有关说法正确的是( )

A.当有0.1mol电子转移时,a极产生1.12L O2(标准状况下)
B.b极上发生的电极反应是:4H2O + 4e- = 2H2↑+ 4OH-
C.d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O
D.c极上进行还原反应,B中的H+可以通过隔膜进入A
如图表示反应M(g)+P(g) nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是
nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是
A.通过分析上图,该反应的正反应为放热反应
B.A状态与C状态的化学反应速率比较为v(A)<v(C)
C.在T 1、D状态时,v正<v逆
D.在T2、B状态时,改变体积始终有v正=v逆,则n=2
相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g)△H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:
2SO3(g)△H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
| A.Q1>Q3>Q2 =78.8kJ |
| B.三个容器中反应的平衡常数均为K=2 |
| C.甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% |
| D.若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=1/(5t) mol/(L·min) |
在相同容积的4个密闭容器中进行同一种可逆反应,2A(g)+B(g)  3C(g)+2D(g),起始时4个容器所盛A、B的量如下表所示: 各容器所盛物质的量
3C(g)+2D(g),起始时4个容器所盛A、B的量如下表所示: 各容器所盛物质的量
| 容器 |
甲 |
乙 |
丙 |
丁 |
| A |
2mol |
1mol |
2mol |
1mol |
| B |
1mol |
1mol |
2mol |
2mol |
在相同温度下,建立平衡时,4个容器中A或B的转化率的大小关系是
A.A的转化率为:甲<丙<乙<丁
B.A的转化率为:甲<乙<丙<丁
C.B的转化率为:甲>丙>乙>丁
D.B的转化率为:丁>丙>乙>甲
将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应3A(g)+B(g)  xC(g)+2D(g),经5 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,用C的浓度变化表示的平均反应速率为0.1 mol·L-1·min-1。下列有关结论正确的是
xC(g)+2D(g),经5 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,用C的浓度变化表示的平均反应速率为0.1 mol·L-1·min-1。下列有关结论正确的是
A.x的值为1
B.用B的浓度变化表示的平均反应速率为0.2 mol·L-1·min-1
C.反应开始前A的物质的量为3 mol
D.5 min时A的浓度为0.2 mol·L-1
反应速率v和反应物浓度的关系是用实验的方法测定的,化学反应H2+Cl2===2HCl的反应速率v可表示为v=k[c(H2)]m[c(Cl2)]n,式中k为常数,m、n值可用表中数据确定。
| c(H2)/mol·L-1 |
c(Cl2)/mol·L-1 |
v/[mol·L-1·s-1] |
| 1.0 |
1.0 |
1.0 k |
| 2.0 |
1.0 |
2.0 k |
| 2.0 |
4.0 |
4.0 k |
由此可推得,m、n值正确的是
A.m=1,n=1 B.m=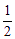 ,n=
,n=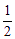 C.m=
C.m=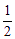 ,n=1 D.m=1,n=
,n=1 D.m=1,n=