(届江苏省南通市高三第二次调研化学试卷)
常温下,用 0.1 mol·L—1HCl溶液滴定10.0 mL浓度为0.1 mol·L—1 Na2CO3溶液,所得滴定曲线如右图所示。下列说法正确的是
| A.当V=0时:c(H+)+c(HCO 3-)+c(H2CO3)=c(OH-) |
| B.当V=5时:c(CO32—)+c(HCO 3-)+c(H2CO3)=2c(Cl-) |
| C.当V=10时:c(Na+)>c(HCO 3-)>c(CO32—)>c(H2CO3) |
| D.当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.在稀硫酸中加入少量氢氧化钠固体,溶液导电性增强 |
| B.饱和碳酸钠溶液中:c(Na+)=2c(CO32-) |
| C.饱和食盐水中:c(Na+) + c(OH-)c(Cl-)+ c(H+) |
| D.pH=12的NaOH溶液中:c(OH-)=1.0×10-2 mol·L-1 |
25℃时,在10mL浓度均为0.1mol/L的NaOH和NH3•H2O混合溶液中滴加0.1mol•L﹣1盐酸,下列有关溶液中粒子浓度关系正确的是
| A.未加盐酸时:c(OH﹣)>c(Na+)=c(NH3•H2O) |
| B.加入10mL盐酸时:c(NH4+)+c(H+)=c(OH﹣) |
| C.加入盐酸至溶液pH=7时:c(Cl﹣)=c(Na+) |
| D.加入20mL盐酸时:c(Cl﹣)=c(NH4+)+c(Na+) |
KO2的晶体结构与NaCl相似,KO2可以看着是Na+的位置用K+代替,Cl-的位置用O2-代替,则下列对于KO2晶体结构的描述正确的是
| A.与K+距离相等且最近的O2-共有8个 |
| B.与K+距离相等且最近的O2-构成的多面体是正八面体 |
| C.与K+距离相等且最近的K+有8个 |
| D.一个KO2晶胞中的K+和O2-粒子数均为8 |
金属晶体中金属原子有三种常见的堆积方式,六方堆积(镁型)、面心立方堆积(铜型)和体心立方堆积(钾型),图(a)、(b)、(c)分别表示这三种晶胞的结构,其晶胞内金属原子个数之比为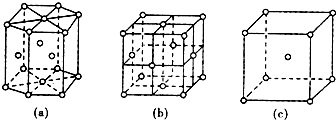
| A.3:2:1 | B.11:8:4 | C.9:8:4 | D.21:14:9 |
有关晶体的结构如图所示,下列说法中不正确的是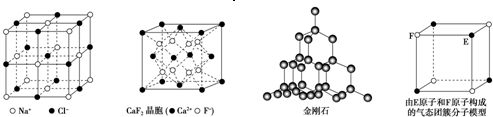
| A.在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
| B.在CaF2晶体中,每个晶胞平均占有4个Ca2+ |
| C.在金刚石晶体中,碳原子与碳碳键个数的比为1:2 |
| D.该气态团簇分子的分子式为EF或FE |