下列操作不能达到目的的是 ( )
| 选项 |
目的 |
操作 |
| A. |
配制100 mL 1.0 mol/L CuSO4溶液 |
将25 g CuSO4·5H20溶于100 mL蒸馏水中 |
| B. |
除去KNO3中少量NaCl |
将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C. |
在溶液中将MnO4-完全转化为Mn2+ |
向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D. |
确定NaCl溶液中是否混有Na2CO3 |
取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
把下列四种X溶液分别加入四个盛有10mL 2mol/L的盐酸的烧杯中,均加水稀释到50mL,此时X溶液和盐酸进行反应,其中反应速率最大的是( )
| A.10mL 4mol/L的X溶液 | B.30mL 2mol/L的X溶液 |
| C.3mL 10mol/L的X溶液 | D.15mL 3mol/L的X溶液 |
N2H4是一种高效清洁的火箭燃料.0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量.则下列热化学方程中正确的是( )
A.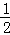 N2H4(g)+ N2H4(g)+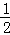 O2(g)= O2(g)=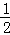 N2(g)+H2O(l)△H=+257kJ•mol﹣1 N2(g)+H2O(l)△H=+257kJ•mol﹣1 |
| B.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣133.5kJ•mol﹣1 |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=+534kJ•mol﹣1 |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJ•mol﹣1 |
在298K、100kPa时,已知:
2H2O(g)═2H2(g)+O2(g)△H1
H2(g)+Cl2(g)═2HCl(g)△H2
2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
| A.△H3=△H1+2△H2 | B.△H3=△H1+△H2 | C.△H3=△H1﹣2△H2 | D.△H3=△H1﹣△H2 |
已知H2(g)+Br2(l)═2HBr(g);△H=﹣72kJ/mol.蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
| H2(g) |
Br2(g) |
HBr(g) |
|
| 1mol分子中的化学键断裂时 需要吸收的能量/KJ |
436 |
a |
369 |
则表中a为( )
A.404B.260 C.230 D.200
已知:(1)H2(g)+ O2(g)═H2O(g);△H="a" kJ/mol
O2(g)═H2O(g);△H="a" kJ/mol
(2)2H2(g)+O2(g)═2H2O(g);△H="b" kJ/mol
(3)H2(g)+ O2(g)═H2O(l);△H="c" kJ/mol
O2(g)═H2O(l);△H="c" kJ/mol
(4)2H2(g)+O2(g)═2H2O(l);△H="d" kJ/mol
下列关系式中正确的是( )
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |