(2014届湖南省十三校高三第二次联考理综化学试卷)
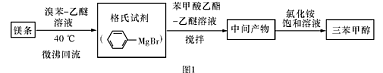
三苯甲醇(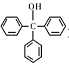 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图所示。
已知:(I)格氏试剂容易水解:
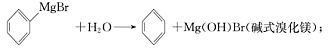
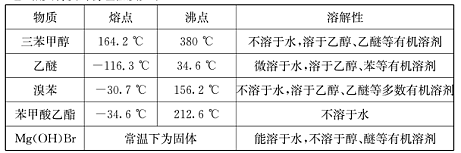
(Ⅱ)相关物质的物理性质如下:
(Ⅲ)三苯甲醇的相对分子质量是260,纯净固体有机物一般都有固定熔点。
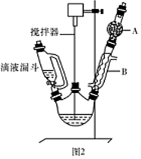
请回答以下问题:
(1)图2中玻璃仪器B的名称: ;装有无水CaCl2的仪器A的作用是 。
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是 ;制取格氏试剂时要保持微沸,可以采用 加热方式。
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写如下空白:

其中,①操作为: ;洗涤液最好选用 (从以下选项中选择);
| A.水 | B.乙醚 | C.乙醇 | D.苯 |
检验产品已经洗涤干净的操作为: 。
(4)纯度测定:称取2.60 g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不反应),充分反应后,测得生成的气体在标准状况下的体积为100.80mL。则产品中三苯甲醇的质量分数为 。
(11分)某中学高一化学兴趣小组的同学,在实验室探究用过量的锌与浓硫酸反应制取SO2。
①这样制取的SO2中可能含有的杂质有________。
②某同学用下列装置连接成一整套实验装置以验证①的判断是否正确,若按气体从左到右流向时,气体流经的各装置导管的编号依次是______→______→______→______→______→(用a、b……填写;每套装置只允许使用一次)。
③根据②确定的实验过程,请将实验时有关装置中所盛药品、实验现象、结论填入下表:
| 装置 |
所盛药品 |
实验现象 |
结论 |
| B |
|||
| C |
CuO固体 |
||
| D |
无水CuSO4 |
实验室利用右图所示装置制取乙酸异戊酯,其合成过程为:
①向圆底烧瓶中加入几粒碎瓷片,并注入0.14mol异戊醇和0.35mol冰醋酸,再加入4 mL浓H2SO4至不再分层。
②在烧瓶上安装冷凝回流装置,加热混合物1小时后,冷却至室温。
③把混合物转至分液漏斗中,加少量蒸馏水,振荡分层后除去水层,再用蒸馏水洗涤有机层。
④用5%的NaHCO3溶液分几次洗涤产品直至中性。
⑤向上述溶液中加NaCl晶体,搅拌静置,对液体进行分液。
⑥将粗产品转至蒸馏烧瓶中,加入碎瓷片,并加适量无水MgSO4或Mg(NO3)2蒸馏,收集135 ℃—143 ℃之间的馏分。
试完成下列问题:
(1)冷凝管中冷却水流向是由_____________进入,由____________流出。(填“A”或“B”)
(2)圆底烧瓶中的物质_______________(填“会”或“不会”)从冷凝管上口跑掉,是因为
_____________________________________________________________________________。
(3)合成实验中浓H2SO4的作用是____________________________________________,碎瓷片的作用是__________________________________________________________________。
(4)乙酸与异戊醇的物质的量之比0.35∶0.14>1∶1的原因是_______________________。
(5)在③中用蒸馏水多次洗涤的作用是_______________________________________。④中用NaHCO3溶液洗涤产品的作用是________________________________________________。
某学生称取9g直链淀粉溶于水,测定淀粉水解的百分率,其程序如下:
淀粉溶液 混合液
混合液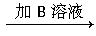 混合液→
混合液→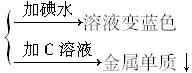
(1)上述实验各步骤所加的试剂为A______________________,B _______________________,C _______________________。
(2)上述测定过程中,只加A溶液,不加B溶液是否可行,理由是___________________。
(3)当析出2.16g金属单质时,淀粉的水解率是___________________________________。
某学生设计了三种实验方案,用以检验淀粉的水解情况
方案甲:淀粉溶液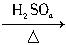 水解液
水解液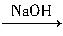 中和液
中和液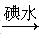 溶液变蓝。结论:淀粉完全没有水解。
溶液变蓝。结论:淀粉完全没有水解。
方案乙:淀粉溶液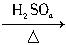 水解液
水解液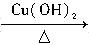 无红色沉淀。结论:淀粉完全没有水解。
无红色沉淀。结论:淀粉完全没有水解。
方案丙:淀粉溶液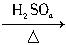 水解液
水解液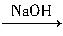 中和液
中和液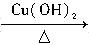 有红色沉淀。结论:淀粉已水解。
有红色沉淀。结论:淀粉已水解。
以上三种方案的设计及结论是否正确?如不正确,请简述理由。
右图为硬脂酸甘油酯在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
(1)在圆底烧瓶中装入7—8 g的氢氧化钠、5 mL硬脂酸甘油酯,然后加入2—3 g的水和10 mL的酒精,加入酒精的作用是________________________________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成。向所得混合物中加入
_________________,静置一段时间,溶液分成上下两层,肥皂在_________________层,此操作名称为_________________。
(3)图中长玻璃管的作用是___________________________________________________。
(4)写出该反应的化学方程式:_______________________________________________。