小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
【提出猜想】放出的气体可能是SO2、O2、H2,提出猜想的依据是 。
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是_____________________________________。
(2)乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式________________________________。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
若拆去B装置,直接连接A和C装置进行实验,可能导致 后果发生。
【实验探究】实验开始时,先将收集到的气体从a通入一段时间后,再点燃C处酒精灯;
这样操作的目的是 。
实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色;
结论:铁粉与硫酸铜溶液反应时,产生的气体是_________________。
【思维拓展】由上述实验可以推出,硫酸铜溶液中可能含有____________。
以下是某研究小组探究影响反应速率部分因素的相关实验数据。
| 实验序号 |
过氧化氢溶液浓度% |
过氧化氢溶液体积/mL |
温度℃ |
MnO2的用量/g |
收集氧气的体积/mL |
反应所需 的时间/s |
| ① |
5 |
1 |
20 |
0.1 |
4 |
16.75 |
| ② |
15 |
1 |
20 |
0.1 |
4 |
6.04 |
| ③ |
30 |
5 |
35 |
 |
2 |
49.21 |
| ④ |
30 |
5 |
55 |
 |
2 |
10.76 |
(1)通过实验①和②对比可知,化学反应速率与有关;从实验和对比可知,化学反应速率与温度的关系是:;
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:
。
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总重量(选填“减小”或“不变”或“增大”)。
某同学为了研究竹子里面气体的成分,做了一个实验。
(1)他先将竹子浸在水里,钻个小孔,看到一串串气泡冒出。然后采用法(填实验室常用的一种集气方法)收集到了甲乙两瓶气体。
(2)将放有足量红磷的燃烧匙伸入甲瓶中(如图)。
用放大镜聚焦,使红磷燃烧,瓶内充满了白烟。然后,将甲瓶倒放水中,松开夹子,结果流入的水约占瓶子容积的1/10。这说明竹子里的气体中肯定含有。
(3)再往乙瓶中倒入一些澄清石灰水,发现石灰水马上变浑浊。这说明竹子里的气体中肯定含有。
(4)那么竹子里的气体含量与空气有什么区别呢?于是,他又用空气重复了上述实验。相比较后得出的结论是:。
从事科学实验的重要环节是进行科学实验设计。科学实验的正确步骤应为:①明确实验目的;②收集有关资料;③设计合理方案;④进行科学实验。请你按照以上四个步骤,完成以下实验设计,根据下图回答问题: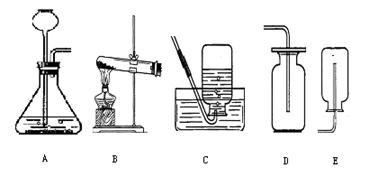
(1)在实验室中用过氧化氢制取氧气。
[ 明确实验目的]:用过氧化氢在实验室里制取氧气。
[ 收集有关资料] 过氧化氢是一种无色液体,在二氧化锰的催化作用下,迅速分解出氧气,其反应的文字表达式为:,反应类型是。
[设计合理方案]:发生装置选用(填序号,下同),收集装置选用。
[进行科学实验]
(2)在实验室中,可以用加热氯酸钾(KClO3)和二氧化锰固体混合物制取氧气。
①[明确实验目的]:。
②[收集有关资料]:氯酸钾是白色的固体,二氧化锰是黑色的固体。且二氧化锰在反应中的作用是。
③设计合理方案:发生装置选用,若选用D收集装置收集氧气,你验证集气瓶中是否已收集满的方法是。
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
⑴红磷在集气瓶中发生反应的文字表达式为。该实验中红磷稍过量,目的是。
⑵待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶体积的,由本实验还可以推知氮气的哪一性质?试写出其中一种。
注意:第(3)题将奖励4分,但化学试卷总分不超过60分。
⑶若将红磷换成硫粉,该实验能否获得成功?,理由是
。
实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:
。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
[提出猜想]除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
[完成实验]按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 |
实验药品 |
分解温度(℃) |
| ① |
氯酸钾 |
580 |
| ② |
氯酸钾、二氧化锰(质量比1:1) |
350 |
| ③ |
氯酸钾、氧化铜(质量比1:1) |
370 |
| ④ |
氯酸钾、氧化铁(质量比1:1) |
390 |
[分析数据、得出结论](1)由实验与实验④对比,证明猜想合理;
(2)实验所用的三种物质,催化效果最好的是。
[反思](3)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和
不变;