下列说法错误的是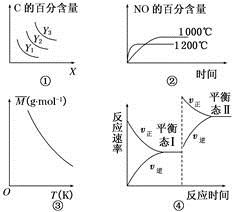
A.对于A(s)+2B(g)  3C(g) ΔH>0,若平衡时C的百分含量跟条件X、Y的关系如图①所示,则Y可能表示温度,X可能表示压强,且Y3>Y2>Y1
3C(g) ΔH>0,若平衡时C的百分含量跟条件X、Y的关系如图①所示,则Y可能表示温度,X可能表示压强,且Y3>Y2>Y1
B.已知可逆反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反应物起始物质的量相同,则图②可表示温度对NO的百分含量的影响
4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反应物起始物质的量相同,则图②可表示温度对NO的百分含量的影响
C.已知反应2A(g)  B(?)+2C(?)-Q(Q>0),满足如图③所示的关系,则B、C可能均为气体
B(?)+2C(?)-Q(Q>0),满足如图③所示的关系,则B、C可能均为气体
D.图④是恒温下某化学反应的反应速率随反应时间变化的示意图,则该反应的正反应是一个气体体积增大的反应
在恒温条件下,向CH3COONa稀溶液中分别加入少量下列物质:其中可使比值
c(CH3COO-)/c(Na+)增大的是
A.固体NaOH B固体KOH.
C. 相同浓度的 CH3COONa稀溶液 D. 氯化钠固体
0.1 mol/L CH3COONa稀溶液中,下列离子浓度关系不正确的是
| A. c(Na+) + c(H+) = c(CH3COO-)+ c(OH-) |
| B. c(Na+) >c(CH3COO->c (OH-)>c(H+) |
| C. c(CH3COO- )+ c(CH3COOH)=" 0.1" mol/L |
| D. c(Na+)>c(CH3COO--)>c (H+)>c(OH-) |
能大量共存于溶液中的离子组有
| A. Al3+、Na+、AlO2-、NO3-、Cl- |
| B. Cl-、HCO3-、OH-、Na+、SO42- |
| C. Ba2+、OH-、Cl-、K+、NO3- |
| D. Fe2+、H+、Na+、NO3-、SO42- |
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示。据图判断正确的是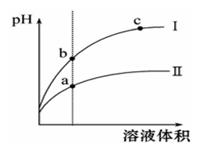
| A.Ⅱ为盐酸稀释时的pH变化曲线 |
| B.b点溶液的导电性比c点溶液的导电性强 |
| C.a点KW的数值比c点KW的数值大 |
| D.b点酸的总浓度大于a点酸的总浓度 |
向50 mL 1 mol/L AlCl3溶液中加入1 mol/L NaOH溶液a mL,充分反应后,生成的沉淀为0.02 mol,a有两个可能的数值,其中一个是180,另一个数值是
| A.40 | B.60 | C.80 | D.90 |