某同学从网络上了解到菠菜中富含可溶性的两类正盐:草酸盐和碳酸盐。该同学欲用实验验证这一事实并检测其中草酸盐的含量。查阅资料得知草酸(H2C2O4)是一种二元有机弱酸,具有较强的还原性;草酸钙(CaC2O4)不溶于水能溶于稀硫酸。请回答下列问题:
(1)该学生将菠菜研磨成粉末、热水浸泡、过滤得到澄清溶液A。研磨菠菜使用的实验仪器的名称为 。
(2)设计实验方案验证菠菜中含有草酸盐和碳酸盐,补充完成预期现象和结论。
| 实验步骤 |
预期现象和结论 |
| 步骤1:调节溶液A至弱碱性,滴加足量CaCl2溶液。 |
①出现白色沉淀,说明菠菜中 。 |
| 步骤2:取步骤1的沉淀于试管中,加入足量的稀硫酸,沉淀完全溶解,并将产生的无色无味的气体通入澄清石灰水中。 |
② 。 |
| 步骤3:向步骤2得到的溶液中滴加几滴高锰酸钾溶液。 |
③ 。 |
(3)欲准确测定菠菜中草酸盐的含量
①操作:取m g菠菜样品,将其中草酸盐全部转化为CaC2O4沉淀分离出来置于烧杯中,用过量的稀硫酸完全溶解后,溶液转入 中并加水配制成250mL溶液。每次移取25.00mL该溶液于锥形瓶中,用0.0100mol·L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。KMnO4滴定实验时发生的离子方程式为 。
②计算:菠菜中草酸盐(以C2O42-计算)的质量分数为(可以只列式不化简) 。
③误差分析: 下列操作会使测定结果偏高的是 。
A.配制溶液时未洗涤烧杯和玻璃棒就加水定容
B.锥形瓶未干燥就加入待测液进行滴定
C.未用标准液润洗就加入标准液开始滴定
D.滴定前尖嘴处有气泡滴定后气泡消失
E.滴定后俯视读数
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下: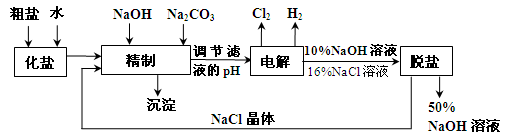
依据上图完成下列问题:
在电解过程中,阴极上生成气体的电子式为。
(2)精制过程中除去阳离子中的Ca2+、Mg2+等杂质,除去Mg2+的离子方程式为。
(3)精制过程要除去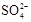 ,可选择下列溶液中的(填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图上(精制过程中加入试剂从左到右的顺序为先后顺序)。
,可选择下列溶液中的(填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图上(精制过程中加入试剂从左到右的顺序为先后顺序)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)在实际生产中也可以用BaCO3除去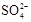 (已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释:。
(已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释:。
(5)脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、、(填操作名称)而制得50%的NaOH溶液。
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了 加成反应。乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。
请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式、。
(2)甲同学设计的实验(填能或不能)验证乙炔与溴发生加成反应,其理由是
(a)使溴水褪色的反应,未必是加成反应
(b)使溴水褪色的反应,就是加成反应
(c)使溴水褪色的物质,未必是乙炔
(d)使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是,它与溴水反应的化学方程式是;在验证过程中必须将此杂质全部除去。
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品。

合成氨的流程示意图如下:
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是____________、____________;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学方程式________________________,__________________________。
(2)设备A中含有电加热器,触媒和热交换器,设备A的名称是________,其中发生的化学反应方程式为__________________________。
(3)设备B的名称为________,其中m和n是两个通水口,入水口是________(填“m”或“n”)。不宜从相反方向通水的原因是________________________________________。
(4)设备C的作用是____________________________________________。
(5)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
已知1 000 K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于________。
将下列家庭常用药物与相应作用连线。
板蓝根冲剂伤口消炎
甘草片退热止痛
红霉素抑制胃痛、助消化
扑尔敏抗菌消炎
阿司匹林治疗感冒
碘酒镇咳化痰
胃舒平抗过敏
在 中用虚线标示出氨基酸形成肽键时断裂化学键的位置。
中用虚线标示出氨基酸形成肽键时断裂化学键的位置。