设NA是阿伏加德罗常数的数值,下列说法正确的是
| A.0.1 mol羟基中含有的电子数为0.7 NA |
| B.28g Fe与足量稀硝酸反应,转移的电子数为NA |
| C.将58.5g NaCl溶于1 L水中,溶液中所含Na+和Cl-总数为2NA |
| D.0.5 mol/LAl2(SO4)3溶液中含有SO42-的数目为1.5 NA |
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
① Sn(s、白) + 2HCl(aq)= SnCl2(aq)+ H2(g)△H1
② Sn(s、灰) + 2HCl(aq)= SnCl2(aq)+ H2(g)△H2



|
③ Sn(s、灰) Sn(s、白)△H3=" +" 2.1kJ/mol
下列说法正确的是高温下,某反应达平衡,平衡常数K=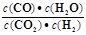 .恒容时,温度升高,H2浓度减小。下列说法正确的是
.恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
| D.该反应化学方程式为CO+H2O=CO2+H2 |
在相同温度和压强下,对反应CO2(g)+H2(g) CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
 |
CO2 |
H2 |
CO |
H2O |
| 甲 |
amol |
amol |
0mol |
0mol |
| 乙 |
2amol |
amol |
0mol |
0mol |
| 丙 |
0mol |
0mol |
amol |
amol |
| 丁 |
amol |
0mol |
amol |
amol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B.乙>丁>甲>丙
C.丁>乙>丙=甲 D.丁>丙>乙>甲
一定温度下,可逆反应A2(s)+3B2(g) 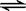 2AB3(g)达到平衡的标志是
2AB3(g)达到平衡的标志是
| A.容器内每减少1mol A2,同时生成2mol AB3 |
| B.容器内每减少1mol A2,同时消耗3mol B2 |
| C.混合气体总的物质的量 |
| D.密闭容器内的物质的质量不再改变 |
在容积固定的密闭容器中存在如下反应: A(g)+3B(g) 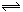 2C(g)该反应正反应为放热反应。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是
2C(g)该反应正反应为放热反应。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是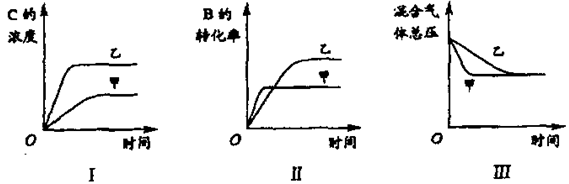
| A.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| B.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
| C.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
| D.图I研究的是压强对反应的影响,且乙的压强较高. |