下列各项比较中前者高于(或大于或强于)后者的是
| A.CCl4和SiCl4的熔点 |
B.邻羟基苯甲醛(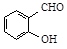 )和对羟基苯甲醛( )和对羟基苯甲醛( )的沸点 )的沸点 |
| C.SO2和CO2在水中的溶解度 |
| D.H2SO3和H2SO4的酸性 |
设N0为阿伏加德罗常数的值。下列叙述正确的是( )。
| A.1.0 L 1.0 mol·L-1的NaAlO2水溶液中含有的氧原子数为2N0 |
| B.12 g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| C.25 ℃时pH=13的NaOH溶液中含有OH-的数目为0.1N0 |
| D.1 mol的羟基与1 mol的氢氧根离子所含电子数均为9N0 |
如图所示,两个连通容器用活塞分开,左右两室体积相同,左室充入一定量NO,右室充入一定量O2,且恰好使两容器内气体密度相同。打开活塞,使NO与O2充分反应,下列判断正确的是(不考虑NO2转化为N2O4)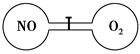
| A.开始时左右两室中的分子数相同 |
| B.反应前后左室的压强相同 |
| C.反应后容器内的密度与反应前的相同 |
| D.反应后容器内无O2存在 |
德国著名行业杂志《应用化学》上曾刊登文章介绍:某中德联合研究小组设计制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。下列说法正确的是 ( )。
| A.水、双氧水、水玻璃都是纯净物 |
| B.石墨和C60互为同素异形体 |
| C.磷酸钙中所含元素都是短周期元素 |
| D.一定条件下石墨转化为C60是化学变化 |
金属及其化合物的转化关系是化学学习的重要内容之一。下列各组物质的转化关系中不全部是通过一步反应完成的是( )。
下列说法中不正确的是 ( )。
| A.分散质微粒直径介于1~100 nm之间的分散系称为胶体 |
| B.在水溶液里或熔融状态下能够导电的化合物中一定是离子化合物 |
| C.液态氯化氢、熔融氧化铝、固体硫酸钡都是电解质 |
| D.非金属氧化物不一定是酸性氧化物,有些金属氧化物也可能是酸性氧化物 |