有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是( )
①在标准状况下,每消耗5.6L CH4可以向外电路提供2mole-
②通过甲烷电极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O
③通过甲烷的电极为电池的正极,通过氧气的电极为负极
④电池放电后,溶液碱性增强
| A.①② | B.①③ | C.①④ | D.③④ |
NA表示阿伏伽德罗常数,下列判断正确的是()
| A.标准状况下,1L液态水中含有的H+数目为10-7NA |
| B.常温常压下,16g CH4中的分子数为NA |
| C.1L 0.2mol/L的FeCl3溶液中Fe3+的数目为0.2NA |
| D.含NA个Na+的Na2O溶解于lL水中,Na+的物质的量浓度等于1 mol/L |
从日本福岛核电站泄漏的放射性物质中,大量存在一种叫做“碘一13l”的放射性元素。下列关于13153I和12753I的说法正确的是()
| A.13153I和12753I都含有55个中子 |
| B.13153I和12753互为同位素 |
| C.13153I和12753I的核外电子数不同 |
| D.13153I和12753I分别含有131和127个质子 |
有A、B、C、D四种金属。将A与B用导线连接起来浸入稀硫酸中,B上有气泡产生;将A、D分别投入到等浓度的稀盐酸中,D比A反应剧烈;将Cu浸入B的盐溶液中,无明显变化;如果把Cu浸入C的盐溶液中,有金属C析出。据此判断它们的活动性由强到弱顺序是
A.C>B>A>D B.D>A>B>C C.D>B>A>C D.B>A>D>C
在一定温度下,下列叙述不是可逆反应A(g)+3B(g) 2C(g)达到平衡的标志的是()
2C(g)达到平衡的标志的是()
(1)C的生成速率与C的分解速率相等; (2)单位时间内有amol A生成,同时生成3amol B;
(3)A、B、C的浓度不再变化;(4)混合气体的总压强不再变化;
(5)混合气体的物质的量不再变化;(6)单位时间消耗amol A,同时生成3amol B;
(7)υA: υB: υC为1:3:2。
A.(2)(4)(5) B.(2)(7) C.(1)(3)(4) D.(5)(6)(7)
下列说法错误的是
A.在C(s) +H2O(g) 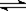 CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率 CO(g) + H2(g)反应体系中,增加碳的量不能迅速提高正反应速率 |
| B.钾的金属性比钠强,所以钾与水的反应比钠的反应剧烈 |
| C.在压强相同条件下,结构相似的CH4、SiH4、GeH4的沸点依次升高,所以结构相似的HF、HCl、HBr、HI的沸点也依次升高 |
| D.面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸 |