对可逆反应4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
| A.达到化学平衡时,υ正=υ逆=0 |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态 |
| C.达到化学平衡时,若增大容器体积,则正反应速率减少,逆反应速率增大 |
| D.达到化学反应平衡后,改变条件当υ正>υ逆,平衡向正反应方向移动 |
吸食或注射毒品会危及人体健康。下列各组物质中都属于毒品的是
| A.冰毒、黄连素 | B.味精、麻黄碱 |
| C.纤维素、尼古丁 | D.海洛因、冰毒 |
咖啡酸是一种具有止血、镇咳、祛痰等疗效的物质,其结构如图所示。据此判断咖啡酸属于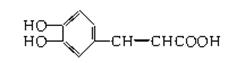
| A.有机物 | B.无机物 | C.氧化物 | D.碳氢化合物 |
Mg(OH)2在下列四种情况下,其溶解度最大的是
| A.在纯水中 |
| B.在0.1 mol·L-1的CH3COOH溶液中 |
| C.在0.1 mol·L-1的NH3·H2O溶液中 |
| D.在0.1 mol·L-1的MgCl2溶液中 |
红葡萄酒密封时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。下列能与乙醇反应生成酯的物质是
| A.苯 | B.乙烯 | C.乙酸 | D.甲烷 |
酸雨的pH小于5.6,下列气体排放会形成酸雨的是
| A.N2 | B.CO2 |
| C.SO2 | D.氟氯代烷 |