据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如右图所示。下列说法正确的是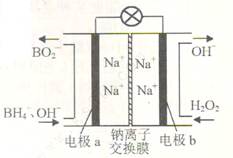
| A.电池放电时Na+从a极区移向b极区 |
| B.每消耗6molH2O2转移电子6mol |
| C.电极a采用MnO2,MnO2既作电极又有催化作用 |
| D.该电池的负极反应为:BH4-+2H2O-8e-=BO2-+8H+ |
25 ℃时,向c mL pH=a的盐酸中滴加pH="b" 的NaOH溶液10 c mL,溶液中Cl-的物质的量恰好等于加入Na+的物质的量,则此时a+b的值为()
| A.13 | B.14 |
| C.15 | D.无法确定 |
把99.5 mL 0.1 mol·L-1 NaOH溶液加到100.5 mL pH=1的H2SO4溶液中,所得溶液的pH为()
| A.2.7 | B.3 |
| C.3.3 | D.11.3 |
等量苛性钠溶液分别用pH为3和4的醋酸中和,设消耗醋酸的体积依次为Va和Vb,则两者的关系正确的是()
| A.Va>10Vb |
| B.Vb=10Va |
| C.Vb<10Va |
| D.Vb>10Va |
用1.0 mol·L-1 NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积关系如图3-5所示。原硫酸溶液的物质的量浓度和反应后溶液的总体积是()
图3-5
| A.1 mol·L-1,60 mL |
| B.0.5 mol·L-1,80 mL |
| C.0.5 mol·L-1,40 mL |
| D.1 mol·L-1,80 mL |
常温下,下列溶液c(H+)="0.01" mol·L-1的是()
| A.0.01 mol·L-1 CH3COOH溶液 |
| B.10-3 mol·L-1 H2SO4浓缩到原体积的110. |
| C.pH=1的H2SO4稀释10倍 |
| D.c(OH-)=10-2 mol·L-1的某溶液 |