根据下图回答问题。
(1)实验仪器a的名称是 。
(2)实验室用高锰酸钾制取氧气的化学方程式为 ,所选用的发生装置
是 (填字母序号,下同)。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气时,二氧化锰起 作用,所选用的收集装置是 或 。
请运用你在初中学过的化学知识和技能,解决下列生活中的实际问题:
(1)家用煤炉中的蜂窝煤有12孔、14孔,甚至16孔等多个品种,孔道越多燃烧越充分,理由是;
(2)铝能制成箔做包装品材料的原因是 ;
(3)除去保温瓶内胆中的水垢,可选用厨房中的;
(4)切过咸菜的菜刀(未清洗擦干)更易生锈,原理是;
(5)油锅着火时可以倒入洗过的蔬菜来灭火,其中的道理是
如图为A、B、C在水中的溶解度曲线图: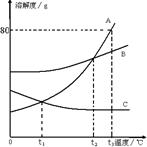
(1)A、C交点的意义是;
(2)t3℃时,A、B、C三者的溶解度由大到小的顺序是 _______________;若在该温度时将45克A放入50克水中, 形成的溶液是__溶液(填“饱和”或“不饱和”);
(3)如果有A、B的混合物(含少量的B),将A提纯的方法是;
(4)t2℃时,等质量的A、B、C三种物质的饱和溶液,温度升高到t3℃,所得溶液溶质质量分数由大到小的顺序是:。
硫酸、盐酸、硝酸是工业上常用的三种酸
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有性;
(2)对于硫酸而言,溶质的质量分数越大,溶液的酸性越强。常温下,10%的稀硫酸的pH______(填“大于”“小于”或“等于”)2%的稀硫酸的pH;
(3)如果要使稀硫酸的pH升高。你采取的化学反应的方法有(要求所选的物质类别不同): ______________;_______________;
(4)盐酸的下列用途中,不能用硫酸代替盐酸的是(填编号)。
①金属表面除锈②制造药物氯化锌③除去NaCl中的少量NaOH
北京时间2013年12月2日1时30分,我国在西昌卫星发射中心用“长征三号乙”运载火箭,成功将“嫦娥三号”探测器发射升空。“长征三号乙”运载火箭(CZ-3B),简称长三乙,是中国目前运载能力最大、技术最先进、构成最复杂的运载火箭。它使用液态四氧化二氮(N2O4)和偏二甲肼(C2H8N2)作为推进剂
(1)有关偏二甲肼的说法不正确的是;
a.偏二甲肼是氧化物 b.偏二甲肼的相对分子质量是60
c.偏二甲肼由12个原子构成
(2)四氧化二氮(N2O4)中氮元素的化合价_______________;
(3)偏二甲肼和四氧化二氮在点燃条件下反应,生成一种产生温室效应的气体、空气中含量最大的气体和水,同时放出大量的热,试写出反应的化学方程式。
化学符号是化学学习的重要工具, 用化学符号表示
(1)2个铁原子(2)硫酸铁中铁元素显+3价
(3)2个碳酸根离子(4)溶于水使温度显著降低的化合物_____。
(5)地壳中含量最多的金属元素(6)氯化钠是由构成的