下列说法正确的是
①向50mLl8mol·L-1的H2SO4溶液中加人足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45mol
②标准状况下,0.5NA个NO和0.5NA个O2混合气体的体积约为22.4 L
③向溶液中滴入氯化钡溶液,再加稀硝酸能检验溶液中是否含有SO42-
④用丁达尔现象可以区分食盐水和淀粉溶液
⑤在使Al溶解产生H2的溶液中能大量存在:NH4+、Na+、Fe2+、NO3-
| A.①②③⑤ |
| B.①③④ |
| C.④ |
| D.③④ |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.通入足量SO2后的溶液:Na+、NH4+、ClO-、CH3COO- |
| B.加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I- |
| C.水电离出的c(H+) = 10-12 mol·L-1溶液:Na+、HCO3-、SO42- 、NO3- |
| D.澄清透明的溶液中:Na+、K+、MnO4-、[Al(OH)4]- |
下列说法正确的是
| A.族序数等于其周期序数的元素一定是金属元素 |
| B.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素 |
| C.从左到右,第三周期非金属元素得电子能力、最高价氧化物对应水化物的酸性均依次增强 |
| D.从上到下,第VIIA族元素氢化物的热稳定性和还原性均依次减弱 |
X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,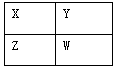
下列说法不正确的是
| A.Y的气态氢化物的稳定性一定比W的强 |
| B.W的原子序数可能是Y的原子序数的3倍 |
| C.Y原子形成的简单离子半径一定比X原子形成的简单离子半径大 |
| D.若Z元素最高价氧化物的水化物是强酸,则W元素的单质具有强氧化性 |
下列实验操作及现象能够达到对碰实验目的的是
| 选项 |
实验操作及现象 |
实验目的 |
| A |
溶液中滴加盐酸酸化氯化钡溶液出现白色沉淀 |
检验溶液中存在SO42- |
| B |
FeBr2溶液加入少量氯水,溶液由浅绿色变为黄色 |
比较Fe2+、Br-还原性强弱 |
| C |
向一定浓度Na2SiO3溶液中通CO2,溶液变浑浊 |
比较C、Si非金属性强弱 |
| D |
将气体通入饱和碳酸钠溶液的洗气瓶 |
除去中CO2的SO2 |
下列各组反应最终有白色沉淀生成的是
①金属钠投入到FeCl2溶液中
②过量NaOH溶液和AlCl3溶液混合
③少量Ca(OH)2投入NaHCO3溶液中
④过量CO2通入Na[Al(OH)4]溶液中
| A.③④ | B.②③④ | C.①③④ | D.①②③④ |