t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)  2Z(g),各组分在不同时刻的浓度如下表:
2Z(g),各组分在不同时刻的浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 2 min末浓度/mol·L-1 |
0.08 |
a |
b |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
下列说法正确的是( )
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率v(Y) =" 0.03" mol·L-1·min-1
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是
A.当有0.1mol电子转移时,a电极产生1.12LH2(标准状况下)
B.b电极上发生的电极反应是: 4H2O+4e-=2H2↑+4OH-
C.c电极上进行的是氧化反应,B池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是: O2+4H++4e-=2H2O
下列实验能达到目的的是
| A.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中含有乙烯 |
| B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡 |
| C.淀粉溶液和稀H2SO4混合加热,加入新制Cu(OH)2悬浊液加热至沸腾,检验淀粉水解产物有还原性 |
| D.利用如图装置并根据有关实验现象能推知酸性强弱:CH3COOH>C6H5OH>H2CO3 |

在一定温度下,向容积不变的密闭容器中充入amolA,发生反应:2A(g) B(g);△H<0。达平衡后再向容器中充入amolA,再次达到平衡后,与原平衡比较,下列叙述不正确的是
| A.相对平均分子质量增大 |
| B.A的转化提高 |
C.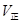 增大, 增大,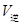 减小 减小 |
| D.反应放出的总热量大于原来的2倍 |
NA为阿伏伽德常数,则下列说法正确的是
| A.在标准状况下,11.2LSO3分子中含有2NA个原子 |
| B.100mL0.1/L的Na2CO3溶液中含有0.01NA个CO32- |
| C.22.4LCl2通入水中充分反应,共转移NA个电子. |
| D.在标准状况下,11.2L的N2和H2组成的混合气中共有NA个原子 |
室温下,下列各组微粒在指定溶液中能大量共存的是
| A.pH=1的溶液中:CH3CH2OH、Cr2O72-、K+、SO42- |
| B.加入铝粉放出大量H2的溶液:Fe2+、Na+、Cl-、NO3- |
| C.NaHCI3溶液中:C6H5O-、CO32-、Br-、K+ |
| D.c(Ca2+)=0.1mol·L-1的溶液中:NH4+、SiO32-、CH3COO-、Br- |