已知(HF)2(g)  2HF(g) ΔH>0,且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) ΔH>0,且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是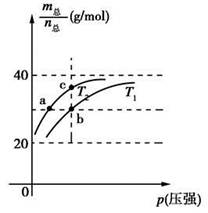
| A.温度:T1<T2 |
| B.平衡常数:K(a)=K(b)<K(c) |
| C.反应速率:vb>va |
D.当 时,n(HF):n[(HF)2]=2:1 时,n(HF):n[(HF)2]=2:1 |
向100 mL FeBr2溶液中通入标准状况下的 Cl2 3.36 L 全部被还原,测得溶液中
c(Br-) =c(Cl-) ,则原FeBr2溶液的物质的量浓度是
A 0.75 mol/LB 1.5 mol/LC 2 mol/L D 3 mol/L
将一定体积的某NaOH溶液分成两等份,一份用pH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用pH=2的一元酸HB溶液中和,消耗酸溶液体积为V2,则下列叙述正确的是
| A.若V1>V2,则说明HA的酸性比HB的酸性强 |
| B.若V1>V2,则说明HA的酸性比HB的酸性弱 |
| C.因为两种酸溶液的pH相等,故V1一定等于V2 |
| D.若将两种酸溶液等体积混合,混合酸溶液的pH一定等于2 |
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度。有关的叙述正确的是
A.H2Y的电离方程式为:H2Y+2H2O 2H3O++Y2- 2H3O++Y2- |
| B.在该酸式盐溶液中c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |
C.HY-的水解方程式为HY-+H2O H3O++Y2- H3O++Y2- |
| D.在该酸式盐溶液中c(Na+)>c(HY-)>c(OH-)>c(H+) |
在25℃时,有80g饱和Ba(OH)2溶液,向其中加入纯BaO粉末a g,反应后温度恢复到25℃,下列有关该溶液的说法正确的是
| A.溶液中c(Ba2+)将增大 | B.溶液的pH将增大 |
| C.溶液中Ba2+总数将减少 | D.溶液中c(OH-)减少 |
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下
(1)CuSO4 + Na2CO3
主要:Cu2+ + CO32-+ H2O → Cu(OH)2↓+CO2↑次要:Cu2+ + CO32-→CuCO3↓
(2)CuSO4 + Na2S
主要:Cu2+ + S2-→ CuS↓次要:Cu2+ + S2-+ 2H2O→Cu(OH)2↓+ H2S↑
据此,下列几种物质溶解度大小比较中,正确的是
| A.Cu(OH)2 > CuCO3 > CuS | B.CuCO3 > Cu(OH)2 > CuS |
| C.CuS > CuCO3 > Cu(OH)2 | D.CuS > Cu(OH)2 > CuCO3 |