常温下,某水溶液中存在的离子有:Na+、B2-、HB-、H+、OH-,存在的分子有H2O、H2B。根据题意回答下列问题:
(1)写出酸H2B的电离方程式 ﹑ 。
(2)常温下,已知0.1 mol·L-1二元酸H2B溶液中c(OH-) / c(H+)=1×10-6。
①常温下,0.1 mol·L-1H2B溶液的pH= ;
②写出该酸(H2B)与少量NaOH溶液反应的离子方程式: ;
(3)常温下,将100 mL 0.1 mol·L-1的稀H2SO4溶液与100 mL 0.4 mol·L-1的NaOH溶液充分混合(溶液体积变化忽略不计),所得溶液的pH= 。
(4)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw= 。该温度下(t℃),0.1 mol·L-1HCl溶液的pH= ;
2005年10月5日,瑞典皇家科学院将本年度诺贝尔化学奖授予法国化学家伊夫·肖万和两位美国化学家罗伯特·格拉布和理查德·施罗克,以表彰他们在烯烃复分解反应研究和应用方面做出的卓越贡献。


伊夫·肖万罗伯特·格拉布理查德·施罗克
烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子——2-丁烯和乙烯:
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。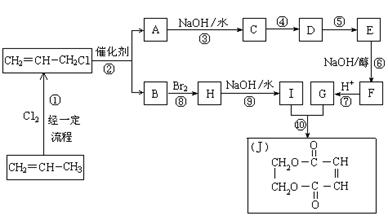
请按要求填空:
(1)写出下列反应的反应类型:
③:,⑥:,⑧:。
(2)反应②的化学方程式是:。
(3)反应④、⑤中有一反应是与HCl加成,该反应是(填反应编号),设计这一步反应的目的是;物质E的结构简式是。
(4)反应⑩的化学方程式是。
A、B、C、D、E、F六种元素均是短周期元素,且原子序数依次增大。B、F原子的最外层电子数均为其电子层数的两倍,D、F元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)转化关系如图(反应条件略去),元素E形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题: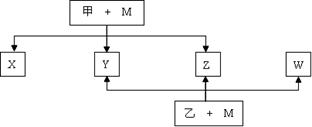
(1)写出M与甲的浓溶液加热时反应的化学方程式。
(2)X、Y、Z、W属于同一类物质,这类化合物固态时的晶体类型为;X、Y、W都能与Z反应,则Z的结构式为。
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=,写出反应的化学方程式。
(4)化合物ED2与元素B形成的某种单质晶体类型相同,且在高温下能发生置换反应。若反应中B的单质被破坏1 mol共价键,则参加反应的化合物ED2的质量为g。
(5)元素B的另一种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12 g该晶体中含有NA个正六边形。
TiO2在工业生产和日常生活中有重要用途。
I.工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:
其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答:(填“需要”或“不需要”)。
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的化学方程式。
答:。
II.TiO2可通过下述两种方法制备金属钛:
“方法一”是电解TiO2来获得Ti(同时产生O2):将处理过的TiO2作阴极,石墨为阳极,熔融CaCl2为电解液,用碳块作电解槽池。
(3)阴极反应的电极反应式为___________________________________。
(4)电解过程中需定期向电解槽池中加入碳块的原因是______________________。
“方法二”是先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti。因下述反应难于发生:
TiO2 (s)+2Cl2 (g) TiCl4(l)+O2 (g)ΔH=+151 kJ·mol-1
TiCl4(l)+O2 (g)ΔH=+151 kJ·mol-1
所以不能直接由TiO2 和Cl2反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
(5)已知:C(s)+O2 (g) = CO2 (g)ΔH=-394 kJ·mol-1。请填空:
TiO2 (s)+C (s)+2Cl2 (g) = TiCl4 (l)+CO2 (g)ΔH= ______________
(6)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因。
答:____________________________________________。
[化学——选修有机化学基础]
某水质稳定剂是由马来酸酐和乙酸乙烯酯聚合而成,可有效防止水垢的产生。
(1)马来酸酐可由马来酸分子内脱水制得。马来酸酐分子中含有五个原子构成的环状结构;马来酸的相对分子质量为116,实验式为CHO,其核磁共振 氢谱显示有两个波峰,面积比为1 : 1。
氢谱显示有两个波峰,面积比为1 : 1。
①马来酸的分子式为。
②马来酸不能发生的反应是(填写序号)。
a.加成反应 b.氧化反应 c.消去反应
d.酯化反应 e.水解反应 f.加聚反应
③马来酸酐结构简式为。
(2)已知:Ⅰ.在一定条件下,乙炔能分别与水.乙酸发生加成反应。
Ⅱ.乙烯醇(CH2=CHOH)不能稳定存在,迅速转变成乙醛。
只用乙炔为有机原料合成乙酸乙烯酯(CH3COOCH=CH2),合成路线如下:
写出反应②.③的化学方程式:
②
③
(3)乙酸乙烯酯有多种同分异构体。与乙酸乙烯酯具有相同官能团且能发生银镜反应的同分异构体有种。
[选修一物质结构与性质]
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
| M |
N |
|
| 第一电离能(kJ/mol) |
495.8 |
418.8 |
回答下列问题:
(1)Z元素原子的价层电子的轨道表示式为:;
(2)由X、Y形成的Y2X2分子中,含有个 键,个
键,个 键:
键:
(3)比较ME、NE的熔点高低并说明理由。
(4)Y、Z、Q的第一电离能由小到大的顺序为。(用元素符号回答)
(5)YQ2中心原子的杂化方式为___________,有一种与YQ2互为等电子体的离子,能用于鉴别Fe3+,写出其电子式________________。
(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有个;GE晶体的密度为ag·cm-3,则晶胞的体积是(只要求列出计算式)。