G 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
(1)写出G中含氧官能团的名称
(2)B→C的反应类型是 。
(3)E的结构简式是
(4)写出F和过量NaOH溶液共热时反应的化学方程式:
(5)某芳香化合物是G的同分异构体,写出同时符合下列条件的该同分异构体的结构简式 (写一种)
①遇氯化铁溶液显紫色 ②能发生银镜反应和水解反应 ③有四种不同化学环境的氢原子
(6)已知(1) (2)苯酚具有还原性,易被硝酸等氧化剂氧化
(2)苯酚具有还原性,易被硝酸等氧化剂氧化
根据已有知识并结合流程中相关信息,写出以苯酚和乙醇为主要原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
CH3CH2Br  CH2=CH2
CH2=CH2
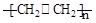
乙醇汽油作为一种新型清洁燃料,是目前世界上可再生能源的发展重点,而且具有较好的经济效益和社会效益,终将成为汽油和柴油的替代品。
(1)写出乙醇完全燃烧的化学方程式:______________________________。
(2)乙醇燃烧时如果氧气不足,可能还有CO生成。用如图装置验证乙醇的燃烧产物中有CO、CO2、H2O,应将乙醇的燃烧产物依次通过(按气流从左到右的顺序填装置编号)________。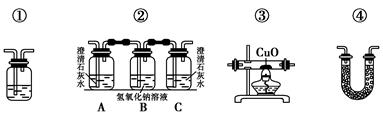
(3)实验时可观察到装置②中A瓶的石灰水变浑浊。A瓶溶液的作用是________;B瓶溶液的作用是________;C瓶溶液的作用是_________________________。
(4)装置③的作用是________;装置①中所盛的是________,作用是______________________。
(5)装置④中所盛的固体药品是________,它可以验证的产物是________。
(6)尾气应如何处理?_________。
(7)海底有大量的甲烷水合物。等质量的甲烷和乙醇完全燃烧产生温室气体CO2较多的是________。
在下列各组气体中,试分析判断哪种气体更易液化?
①Cl2、N2;②SiH4、CH4;③SO2、CO2;④邻二甲苯、对二甲苯;⑤甲烷、乙烷;⑥丁烷、异丁烷
已知M2+3d轨道上有5个电子,试推出:
(1)M原子的核外电子排布。
(2)M原子的最外层和最高能级组中电子数各为多少?
(3)M元素在周期表中的位置。
由下列元素在周期表中的位置,写出元素原子的价电子排布式。
(1)第4周期ⅥB族;
(2)第5周期ⅠB族;
(3)第5周期ⅣA族;
(4)第6周期ⅡA族;
(5)第4周期ⅦA族。
铁及其化合物之间的相互转化可用下式表示: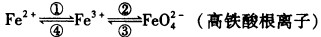
回答下列有关问题:
(1)铁元素位于元素周期表的第四周期第Ⅷ族,原子序数是26,最外层有2个电子。元素铁的原子结构示意图是。
(2)检验硫酸铁溶液中是否存在Fe2+的方法是
(3)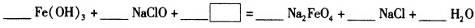
(4)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为Fe3+。Na2FeO4之所以能净水,除了能消毒杀菌外,另一个原因是(结合离子方程式说明) 。