下列有关电解质溶液的说法正确的是
| A.在溶质物质的量浓度相等的Na2A和NaHA溶液中,阴离子总数相等 |
| B.中和等体积pH=11的氢氧化钠溶液,所需pH=3醋酸溶液的体积大于pH=3盐酸的体积 |
| C.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液,浓度关系: c[(NH4)2CO3]<c[(NH4)2SO4]<c(NH4Cl) |
| D.酸式盐NaHA的水溶液呈碱性,离子的物质的量浓度关系:c(Na+)>c(HA—)>c(OH—)>c(H+)>c(A2—) |
某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水。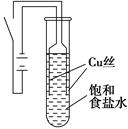
实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
| 物质 |
氯化铜 |
氧化亚铜 |
氢氧化亚铜(不稳定) |
氯化亚铜 |
| 颜色 |
固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 |
红色 |
橙黄色 |
白色 |
*相同温度下CuCl的溶解度大于CuOH
下列说法错误的是
A.反应结束后最终溶液呈碱性
B.阴极上发生的电极反应为:2H2O + 2e-¯ ═ H2↑+ 2OH-¯
C.电解过程中氯离子移向阳极
D.试管底部红色的固体具有还原性
常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计),则下列说法错误的是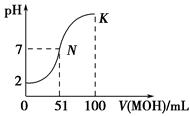
| A.常温下,MA的水溶液的pH=a,由水电离产生的c(H+)=1×10-a mol·L-1 |
| B.在K点,水溶液中存在:c(M+) = 2c(A-) |
| C.在N点,水溶液中存在:c(M+) + c(H+)= c(A-)+ c(OH-) |
| D.在K点,若此时溶液的pH=10,则c(MOH)+c(M+)=0.01mol·L-1 |
25℃时,溶液只含有Na+、H+、OH-、CH3COO-这四种离子,下列说法错误的是
| A.溶液只能是CH3COONa溶液 |
| B.溶液中的离子浓度可能是c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C.溶液中的离子浓度可能是c(Na+)> c(CH3COO-)> c(OH-)>c(H+) |
| D.溶液中的离子浓度可能是c(Na+)> c(OH-)> c(CH3COO-)> c(H+) |
下列各组离子一定能大量共存的是
| A.含大量Fe3+的溶液中:NH4+、Mg2+、Cl-、HSO3- |
| B.加入Al有H2生成的溶液中:Na+、K+、Cl-、NO3- |
| C.NaOH溶液中:K+、Na+、AlO2-、CO32- |
| D.NaHCO3溶液中:K+、Al3+、Cl-、SO42- |
下列离子方程式正确的是
| A.电解氯化镁溶液:2Cl-¯+ 2H2O ═ 2OH¯- + H2↑+ Cl2↑ |
| B.将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C.将少量CO2气体通入苯酚钠溶液中:2C6H5O- + CO2 + H2O→2C6H5OH +CO32- |
| D.硫酸亚铁酸性溶液中加入过氧化氢:2Fe2+ + H2O2 +2H+ = 2Fe3+ + 2H2O |