碳、氢、氮、氧四种元素对动、植物的生命活动有着重要的意义。
(1)糖类是人类食物的重要成分,例如蔗糖(C12H22O11)是食品常用的甜味剂,蔗糖属于 (填字母序号)。
A.氧化物 B.无机物 C.有机物 D.混合物
(2)“每日氢元素”是目前世界上抗氧化食品中公认的里程碑式产品,原因是它能与人体内多余的氧元素结合成人体所需的营养物质 。
(3)人体通过食物获得蛋白质。
①下列食品富含蛋白质的是 (填字母序号)。
A.鸡蛋 B.米饭 C.苹果 D.西红柿
②蛋白质在胃肠内与水反应生成氨基酸。氨基酸进入血液循环后一部分被氧化,生成尿素[CO(NH2)2]等排出体外。从植物生长所需元素看,尿素属于化肥中的 肥。
③ 甘氨酸(CH2NH2COOH)是人体所需的一种氨基酸,请将甘氨酸在人体内反应的化学方程式补充完整:2CH2NH2COOH + 3O2 酶CO(NH2)2 + 3H2O + 3 。
为了书写和学术交流的方便,化学上通常用一些化学符号表示物质、粒子等,请用化学符号填空:
(1)能进入人体血液中的亚铁离子;(2)保持二氧化碳化学性质的微粒:;
(3)氧化镁中镁元素显正二价:。(4)农村大力推广使用的沼气(又名天然气)的主要成分。
某碳酸钠样品中含有少量氯化钠杂质,为测定该样品中碳酸钠的质量分数,进行了如下实验:
① 实验一: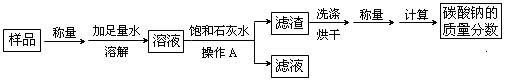
请回答下列问题:
(Ⅰ)操作A中用到玻璃棒,其作用是 。
(Ⅱ)甲同学取少量(碳酸钠样品)溶液,滴入无色酚酞试液,溶液由无色变成 。
(Ⅲ)在实验过程中加入饱和石灰水后发生反应的化学方程式是。
(Ⅳ)为探究上述反应后滤液中的溶质成分,乙同学向滤液中滴加过量稀盐酸,发现
有气泡产生,则滴加盐酸前滤液中的溶质除氯化钠外还有。
② 实验二:
丙同学取12g该碳酸钠样品放入烧杯中,加入100g稀盐酸(足量),完全反应后, 所
得溶液质量为107.6 g。试计算:
(Ⅰ)生成二氧化碳物质的量为mol。
(Ⅱ)碳酸钠样品中Na2CO3的质量分数。(写出计算过程,保留到0.1%)
(Ⅲ)如果测得的结果比实际的质量分数高,可能的原因是。(答一种即可)
请根据下列装置回答有关问题: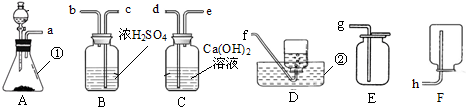
(1)有标号仪器的名称:①;②。
(2)若用上述装置制取二氧化碳,则A中发生反应的化学方程式为。要制取和收集一瓶干燥的二氧化碳气体,其装置接口的连接顺序是(用接口字母顺序从左至右连接)。检验二氧化碳是否集满的方法是。结果发现小木条始终不灭,出现这种情况的原因可能是(写出其中1种)。
(3)A改成启普发生器制取二氧化碳会更好,启普发生器优点是。
现有银、铜、铁三种金属,某研究小组为探究银、铜、铁的金属活动性顺序,设计了三
个实验:(Ⅰ)将铁片浸入稀硫酸中;(Ⅱ)将银片浸入稀硫酸中;(Ⅲ)将铁片浸入硫酸铜溶液中。
实验(Ⅲ)中反应的化学方程式为;该反应的基本类型为反应
上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象)。根据以上探究,三种金属的活动性由强到弱的顺序是。
用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如下图所示: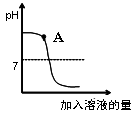
① 该实验是将(填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
② A点溶液中的溶质为。
③ 要测出反应过程中溶液的PH,应如何操作。