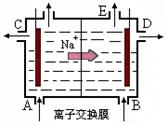
(1)右图为阳离子交换膜法电解饱和食盐水(滴有酚酞)原理示意图,E口产生H2,电解食盐水的离子方程式为: ,溶液变红色的是: 区(填A或B)。
(2)电化腐蚀是钢铁发生腐蚀的主要原因,又可分为吸氧腐蚀和析氢腐蚀,发生吸氧腐蚀的电极反应式:负极 正极
(3)下图是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计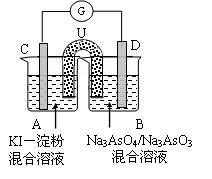
此装置中进行的反应是可逆反应,其反应方程式式为:AsO43-+2I-+H+ AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 D电极上的电极反应式为
AsO33-+I2+H2O,向B杯中加入适量较浓的硫酸,发现G的指针向右偏移。此时A杯中的主要实验现象是 D电极上的电极反应式为
实验室里通常用 MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:
MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:
MnO2 + 4HCl(浓) △MnCl2 + Cl2↑+ 2H2O
(1)在该反应中,如有1 mol Cl2生成,被氧化的HCl的物质的量是mol,转移电子的物质的量是mol 。
mol Cl2生成,被氧化的HCl的物质的量是mol,转移电子的物质的量是mol 。
(2)某温度下,将Cl2通入NaOH溶液中,反应得到的混合液中ClO- 与ClO3- 物质的量之比为1∶1 ,反应的化学方程式是。
将 分别含有MnO4—、Fe3+、Fe2+、I—的四种溶液混合,调节溶液的pH值,使pH=1,充分反应后:
分别含有MnO4—、Fe3+、Fe2+、I—的四种溶液混合,调节溶液的pH值,使pH=1,充分反应后:
(1)若I—离子有剩余,则上述四种离子在溶液中还存在的有,一定不存在的是;
(2)若所得混合液呈紫色,则上述四种离子在溶液中一定存在的有,一定不存在的离子有;
某钠盐溶液可能含有阴离子NO3—、CO32—、SO32—、SO42—、Cl—、Br—、I—。为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
根据上述实验判断,原溶液中一定存在的阴离子为,一定不存在的阴离子为 ,可能存在的阴离子为。
,可能存在的阴离子为。
按要求写出下列反应的化学方程式或离子方程式
(1)钢铁工业是国家工业的基础。请回答:
①写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
②在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。
写出铁粉和水蒸气反应的化学方程式:
(2)铝片放入NaOH溶液中有气体生成,写出反应的离子方程式:
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。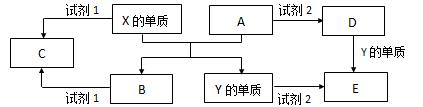
(1)Y元素在元素周期表中的位置周期族
(2)X的单质与A反应的化学方程式是。
(3)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是。
(4)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成, 该反应的化学方程式是。
该反应的化学方程式是。