能源家族成员:①石油 ②电力 ③风能 ④天然气 ⑤水煤气 ⑥氢能, 其中属于二次能源的有
| A.①③⑥ | B.②④⑤ | C.①③④ | D.②⑤⑥ |
设NA为阿伏加德罗常数,则下列说法不正确的是
| A.0.1mol乙炔分子中含有的共用电子对数目为0.5NA |
| B.1.6g甲烷完全燃烧生成二氧化碳和水,转移的电子数为0.8NA |
| C.14g乙烯和环丙烷混合物中含有的碳原子数目为NA |
| D.在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
下列化学用语错误的是
A.羟基电子式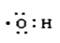 |
| B.乙烯的结构简式 CH2CH2 |
| C.乙酸的实验式 CH2O |
D.3,3-二甲基-1-戊烯的键线式: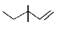 |
下列关于“生活中的化学”的叙述不正确的是
| A.棉花和蚕丝的主要成分都是纤维素 |
| B.误食重金属盐,可立即喝牛奶或鸡蛋清解毒 |
| C.食用植物油的主要成分是高级不饱和脂肪酸甘油酯 |
| D.新居室内装饰材料中缓慢释放出甲醛、甲苯等有机物会污染室内空气 |
现有一混合物的水溶液,可能含有以下离子中的若干种: K+、NH4+、Ba2+、CO32-、Cl-、SO42--。现取两份200 mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36 g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验,以下推测正确的是
| A.一定存在K+、NH4+、CO32-、SO42-,一定不存在Ba2+、Cl- |
| B.一定存在NH4+、Cl-、CO32-、SO42-,可能存在K+ |
| C.c(SO42-)="0.2" mol·L-1,c(NH4+)>c(SO42-) |
| D.如果溶液中存在NH4+、Cl-、CO32-、SO42-、K+五种离子,则c(K+)>0.2 mol·L-1 |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是生活中常用的金属材料。下列说法正确的是
A.原子半径:A<B<C<D<E
B.金属性:D>C
C.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
D.化合物AE与CE含有相同类型的化学键