下图为用镀锌铁片制成的日常用品。镀锌铁是指通过镀锌工艺在铁皮上进行镀锌而制成的一种产品,热镀锌产品广泛用于建筑、家电、车船、容器制造业、机电业等,几乎涉及到衣食住行各个领域。
为测定铁片镀锌层的厚度实验过程如下。
【实验步骤】
⑴ 剪取一片镀锌铁片,量得长度=2.0cm,宽度=1.9cm。
⑵ 用电子天平称量质量0.857g。
⑶ 实验中需要溶质质量分数为10%的稀盐酸200mL(密度=1.05g/mL),需要量取溶质质量分数为37%的浓盐酸(密度=1.18g/mL) mL(保留至小数点后1位),然后稀释。
⑷ 将镀锌铁片放入溶质质量分数为10%盐酸中。当观察到 ,可以判断镀锌层恰好反应。
⑸ 将溶液中的铁片取出清洗、擦干、烘干后用电子天平称量质量0.837g。
【计算结果】
⑴ 铁片镀锌层的质量有 g。
⑵ 已知锌的密度7.1g/cm3,计算出铁片镀锌层厚度mm(保留至小数点后2位)。
【实验反思】
实际计算结果偏大,同学们分析,这是因为很难通过观察现象判断镀锌层恰好反应,造成镀锌铁片浸泡在盐酸中时间 。(填“偏长”、“偏短”)
【实验改进】
资料卡片:如图1所示,两种金属活动性不同的金属放入酸碱盐溶液中,会有电子的流动,从而产生电流。
将上述实验改进成如图2的装置,当观察到 ,此时锌层恰好反应。
实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).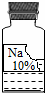
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 ()
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
| 物质 |
NaCl |
NaOH |
Na2CO3 |
NaHCO3 |
| 溶解度g |
36 |
109 |
215 |
9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
| 实验步骤 |
实验现象 |
结论及化学方程式 |
| ①取少量溶液于试管中,②滴加 |
产生大量气泡 |
反应的化学方程式: |
| ③把产生的气体通入澄清的石灰水中. |
澄清的石灰水变浑浊 |
猜想②正确. 反应的化学方程式: |
潜水艇有两种供氧的装置,第一种是储备压缩氧气,第二种是在紧急的情况下才使用的过氧化钠(Na2O2)作供氧剂,小红同学对过氧化钠如何作供氧剂产生浓厚的兴趣,于是他在老师的指导下展开了以下的探究活动。
【查阅资料】
①过氧化钠是用在矿山、坑道、潜水或宇宙飞船等缺氧的场合中,将人们呼出的CO2转换成O2,以供呼吸之用。
②二氧化碳与过氧化钠反应的生成物只有两种,一种是氧气,另一种是化合物。
③人呼出的气体中含有的水分也能与过氧化钠反应生成氧气。
(1)小红利用下图的BCDE装置组合和有关药品制取并收集氧气。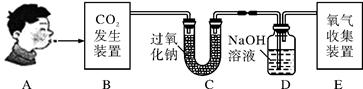
若用大理石与稀盐酸制取二氧化碳,则B中装置可采用上图中的____;E中装置可采用上图中的____ __;B中的化学方程式为: ___________________________。
(2)二氧化碳与过氧化钠反应除生成氧气外还生成什么物质?
【作出猜想】小红作出了以下三种猜想:
①生成碳酸;②生成氢氧化钠;③生成碳酸钠。
通过对反应物有关的元素组成的分析,乙同学认为猜想_______一定是错误的,理由是_________。
【进行实验】
小红通过以下实验验证了另一个猜想的正确性,请完成下述实验报告。
| 实验步骤 |
实验现象 |
实验结论 |
| 取CO2与Na2O2反应后的固体少量于试管中,加入少量__________,把产生的气体通入足量的澄清石灰水中 |
①______________; ②________________ |
猜想____是正确的 |
【反思与交流】
①小红若用图A来代替B装置,证明二氧化碳与过氧化钠反应生成了氧气,你是否同意小红的做法?____(填“是”或“否”),原因:____________________________________。
②由此可知道过氧化钠与二氧化碳反应的化学方程式为:___
有一固体混合物M,已知其中可能含有Ba(OH)2、Na2CO3、Na2SO4、NH4Cl、FeCl3五种物质中的两种或多种。某同学按照下图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行)。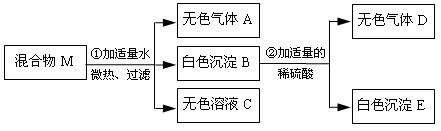
试根据实验过程和现象做出判断,填写以下空白:
(1)气体A的化学式 ;把气体D通入紫色石蕊试液中,石蕊变色。
(2)写出过程②发生反应的化学方程式。
(3)原混合物M里,还不能确定的物质是(写化学式),
要确定它是否存在,请简述你的设计方案:。
(4)农业生产中常用铵态氮肥补充土壤中的氮元素,根据实验步骤①带给你的启示,请你为使用铵态氮肥提出合理化建议:。
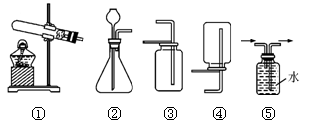
下图为实验室中常见的气体的制备、除杂和性质实验的部分仪器,试根据题目要求,回答下列问题: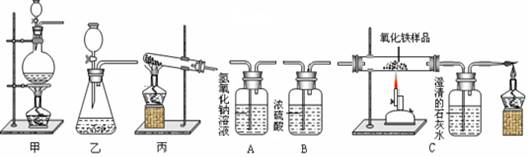
(1)请写出能用装置乙制备的一种气体的化学方程式。检查装置乙气密性的方法是 。
(2)小明同学想研究一氧化碳的还原性,通过查阅资料知道:草酸(H2C2O4)与浓硫酸混合加热会产生一氧化碳,反应方程式为:H2C2O4加热CO↑+ CO2↑+ H2O
①用草酸制取CO,你认为应选择的发生装置是(填“甲”、“乙”或“丙”)。
②要用干燥、纯净的一氧化碳还原氧化铁并测定气体生成物的性质,合理的连接顺序是:草酸加热后的气体生成物
③能证明CO气体具有还原性的实验现象是。
④小明还想计算12g氧化铁样品中氧化铁的质量分数,他收集了以下两组数据(假设所有能发生的反应都反应完全):
数据一:根据参加反应的草酸的质量计算出制得了一氧化碳5.6g。
数据二:反应前后C装置中的盛有澄清石灰水的装置增重6.6g。
请选择合理的一组数据,计算出12g氧化铁样品中氧化铁的质量分数为(最终结果精确到0.1%)。
同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液。已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究: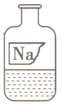
(1)小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是。
(2)他取少量待测液于试管中,加入过量的稀HCl,看到,由此小张同学认为,溶液为Na2CO3溶液。
(3)小李同学对小张同学的结论提出疑问,并进行了以下实验进行验证:取少量待测液于试管中,加入过量的CaCl2溶液,生成白色沉淀,该反应方程式为,静置,(写出还需进行的操作及现象)。
通过实验,小李认为小张结论正确。
(4)二位同学给试剂瓶贴一新标签:Na2CO3。
(5)实验结束后,同学们通过讨论认为试剂瓶原标签也可能不是Na2CO3,你认为他们的理由是。