一包不纯的Na2CO3固体,杂质可能是CaCl2、NaCl、NaHCO3中的一种或几种。现取该样品溶于水得到澄清溶液;另取样品10.6g,加入100g稀盐酸恰好完全反应,产生气体4g,则下列判断不正确的是
| A.加水得澄清溶液,样品中一定没有CaCl2 |
| B.样品中一定含有NaCl,可能含有NaHCO3 |
| C.样品中一定含有NaHCO3,可能含有NaCl |
| D.所加的稀盐酸溶质质量分数小于7.3% |
下列实验操作中能达到实验目的的是
| A.检验氢气纯度时,没有听到任何响声,表明氢气已纯净 |
| B.用适量的水可以区分硝酸铵固体和氢氧化钠固体 |
| C.粗盐提纯实验中,蒸发结晶直到滤液蒸干时停止加热 |
| D.用PH试纸测定溶液酸碱度时,先将PH试纸用水润湿,然后再测定 |
下列混合物,能按“溶解一过滤一蒸发”的步骤加以分离的是
| A.食盐和细砂 | B.水和酒精 |
| C.石灰石和生石灰 | D.蔗糖和味精 |
下列说法不正确的是
| A.档案材料要用碳黑墨水笔填写 |
| B.人的胃液里含有少量的盐酸,可以帮助消化 |
| C.50mL水和50mL酒精混合后,得到l00mL酒精溶液 |
| D.没有密封的饼干在空气中逐渐变软,说明空气中含有水蒸气 |
区分O2、H2、CO2三种气体的最简便的方法是
| A.将气体通入澄清石灰水 | B.将气体通过红热的铜网 |
| C.将气体通过灼热的氧化铜 | D.用燃着的木条伸入集气瓶中 |
在托盘天平的两个托盘上各放一只烧杯,分别注入相同质量分数、相同质量的稀盐酸,天平平衡。向左边的烧杯中加入1 0 g金属锌,向右边的烧杯中加入1 0 g金属镁。当反应停止后,金属都有剩余,天平指针的指向是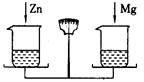
| A.分度盘的左边 | B.分度盘的中间 |
| C.分度盘的右边 | D.3种情况都有可能 |