某小组同学利用如图所示装置探究铁生锈的条件,其中C、D的分液漏斗中为足量且浓度和体积均相同的稀盐酸。
(1)步骤一:关闭K2和K3,打开K1,A中反应的化学方程式是 ,B中所盛放的试剂是 。对比铁丝表面的变化,能够说明铁生锈与水有关的是装置 和 (填C、D或E,下同),能够说明铁生锈的快慢与氧气浓度有关的是装置 和 。
(2)步骤二:关闭K1,打开K2和K3,将装置C、D中分液漏斗内的稀盐酸同时全部注入广口瓶中,两个广口瓶中现象的不同点是:① ;② ,由此也可以判断铁丝生锈情况。C中反应的化学方程式是 。
(3)温度会影响铁生锈的快慢,请设计实验加以证明: 。
在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成C0,那么碳与氧化铜反应生成的气体也有多种可能?”
[猜想]碳与氧化铜反应生成的气体中:①只有CO2②只有CO③既CO2,又有CO。
[查阅资料]浸有磷钼酸溶液的氯化钯试纸遇CO2无变化,但遇到微量CO会立即变成蓝色。
[方案设计]通过上述资料和已有知识,小雨初步设想用浸有磷钼酸溶液的氯化钯试纸和澄清的石灰水对碳与氧化铜反应生成的气体进行检验。根据小雨的设想,请你完成填空:
(1)若试纸不变色,石灰水变浑浊,则只有C02;
(2)若试纸,石灰水,则只有C0;
(3)若试纸,石灰水,则既有CO2,又有CO。
[实验验证]经过思考之后,小雨设计了如图所示实验装置:
实验步骤:
(1)打开弹簧夹,先通一会儿纯净、干燥的N2;
(2)关闭弹簧夹,点燃酒精灯,加热。
结论:小雨通过分析实验现象,确认猜想③是正确的,请你写出装置C中发生反应的化学方程式:;
[反思与评价]
(1)该实验开始通一会儿N2的目的是;
(2)请从环保的角度分析该实验装置的不完善之处。
同学们运用对比的学习方法探究碱的性质。


(1)由上图实验一、二可知,氢氧化钠会吸收空气的,因此要密封保存。
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C, A瓶内发生反应的化学方程式为,对比A瓶与(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应。
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙溶液(分别编号为A、B)。
| 方案一 |
方案二 |
分析 |
| 微热(不考虑水分蒸发) |
两种方案中均观察到A试管内出现白色浑浊,A中试剂为; 方案二的设计原理是利用了。 |
(4)同学们看到盛有NaOH的试剂瓶上标注着“NaOH含量不少于96.0%”,开始如下探究:
【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】工业制取NaOH的反应原理是:2NaCl + 2H2O 2NaOH + H2↑ + Cl2↑,
2NaOH + H2↑ + Cl2↑,
然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
【提出猜想】杂质为碳酸钠和氯化钠。
【实验探究】取样溶于水,并分成两份。
步骤①:向一份溶液中滴加酚酞试剂;
步骤②:向另一份溶液中滴加过量稀硝酸;
步骤③:向②所得溶液中继续滴加硝酸银溶液。
【实验结论】猜想正确。
请分析:
Ⅰ.步骤①中可观察到液体变色;
Ⅱ.步骤②所得溶液中的溶质除NaCl外,还有;
Ⅲ.写出步骤③中发生反应的化学方程式;
Ⅳ.上述实验中步骤(填写序号)是没有必要进行的。
某化学兴趣小组的同学学习了“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
【提出问题】废液中所含溶质是什么?
【猜想与假设】
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl和HCl
猜想4:废液中的溶质是。
【讨论与交流】小明认为猜想1无需验证就知道是错误的,他的理由是。
【实验与结论】
(1)为验证猜想3成立:根据盐酸性质,小王选择如图五种不同类别物质,其中X可以是(填一种具体物质名称或化学式)。
小勇取少量于试管,滴加AgNO3溶液,产生白色沉淀,
再加稀硝酸沉淀不溶解,于是小勇认为猜想3正确,请你评价小勇的结论:。
(2)小丽为验证猜想4成立,可选择的试剂是。
(3)处理废液,回收利用:欲从猜想4的废液中得到纯净NaCl晶体,小芳设计了如下方案:在废液中加入适量Ca(NO3)2溶液,过滤、对滤液蒸发结晶。请评价该方案是否可行?理由。
实验室用98%的浓硫酸配制稀硫酸,并进行相关的性质实验。(夹持仪器省略,装置气密性良好)
(1)配制100g19.6%的稀硫酸的步骤是Ⅰ.;Ⅱ.量取;Ⅲ.溶解。读取水的体积时,视线应与量筒内液体保持水平。
(2)与金属反应实验:锌粒与稀硫酸反应制取氢气
AB CDE
仪器a的名称是,锌粒与稀硫酸反应的化学方程式是。以上五个装置不可能收集到氢气的是(填写字母编号)。比较B、C装置,B装置的优点是。能随时控制反应进行或停止,符合该条件的发生装置是。
(3)鉴别实验:现需鉴别三包失去标签的白色固体,它们可能是碳酸钙、氯化钡、硝酸钾,请
按下表完成实验设计:
| 步骤一: (物理方法) |
取样于三支试管中分别加入 试剂。 |
现象: |
先鉴别出碳酸钙固体 |
| 步骤二: (化学方法) |
再任取一支未鉴别出试剂的试管中滴入稀硫酸 |
现象: |
小明在做实验时发现实验室中有一瓶标签受损的无色液体,如图所示。小明的化学兴趣小组对此产生了疑问。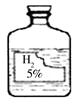
【提出问题】这瓶无色液体是什么呢?
【做出猜想】根据初中所学的化学知识,该液体只能是
过氧化氢溶液、碳酸、稀硫酸和蒸馏水中的一种。
【讨论交流】 大家讨论后一致认为
(1)不可能是蒸馏水,理由是。
(2)不可能是碳酸,理由是碳酸不稳定,易分解。
【实验验证】
为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 |
实验现象 |
实验结论 |
| 步骤一: 取该液体适量于试管中,向其中加入少量粉末 |
没有气泡产生。 |
该液体不是过氧化氢溶液。 |
| 步骤二: 取该液体适量于试管中,向其中滴加少量氯化钡溶液。 |
该液体是稀硫酸。 |
【反思交流】
(1)大家认为标签受损的原因可能是 。
(2)如果该液体是过氧化氢溶液,请用化学方程式表示步骤一中所发生的化学反应:。