亚硝酸钠是一种食品添加剂,按照《食品添加剂使用卫生标准》规定,食品中允许添加限量为70mg/kg,不可超量、超范围使用。亚硝酸钠外观酷似食盐且有咸味,如果将亚硝酸钠(NaNO2)误作食盐食用或摄入过量亚硝酸盐后,可引起中毒,甚至死亡。亚硝酸钠和食盐的有关资料如下:
| 项目 |
亚硝酸钠(NaNO2) |
氯化钠(NaCl) |
| 水溶性 |
易溶,在15℃时溶解度为81.5g |
易溶,在15℃时溶解度为35.8g |
| 熔 点 |
271℃ |
801℃ |
| 沸 点 |
320℃会分解,放出有刺鼻气味的气体 |
1413℃ |
| 跟稀盐酸作用 |
放出红棕色的气体NO2 |
无反应 |
(1)根据上表提供信息,请写出鉴别亚硝酸钠和食盐的两种方法:
① ;
② 。
(2)亚硝酸钠有咸味,外形与食盐很相似,其水溶液显碱性,食盐的水溶液呈中性。根据以上叙述,鉴别亚硝酸钠溶液和食盐溶液应选用的试剂是 。
(3)亚硝酸钠跟盐酸反应会生成氯化钠、两种氮的氧化物(NO2、NO)和水,请你写出亚硝酸钠跟盐酸反应的化学方程式为 。
下图是小华配制100g溶质质量分数为7.5%的NaCl溶液的实验操作示意图: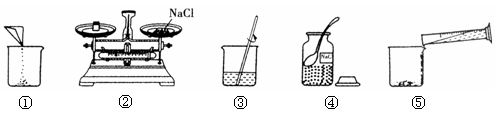
(1)上图中的玻璃仪器分别是广口瓶、量筒、 和玻璃棒,其中玻璃棒在此操作中的作用是 。
(2)指出图②中的一处错误操作 。
(3)通过计算确定需要水的质量是 g,配制时应选择 (填10、50或100)mL的量筒量取所需要的水。
(4)下列错误操作可能导致溶液溶质的质量分数小于7.5%的是_____________(填序号)
| A.②操作中食盐与砝码放置颠倒; |
| B.①操作中有固体洒落; |
| C.⑤操作中有水溅出; |
| D.读取量筒内液体体积于视线过低; |
E、装瓶存放操作中溶液洒落。
(5)该同学在称量氯化钠药品前天平的指针偏左,则所配制的溶液的质量分数 (填“偏大”“偏小”“不受影响”)
小明在实验室做加热硫酸铜晶体试验的过程中,试管炸裂,请你分析一下可能的原因。(至少两个原因)
(1) 。
(2) 。
正确的操作能保证实验顺利进行。请填写下列有关实验操作中的空格:
(1)用酒精灯给物质加热时,要用酒精灯火焰的_______________;
(2)给试管加热时,都要先要给试管______________,再加热;
(3)用量筒量取液体度数时,视线与___________保持水平。
下表为元素周期表中部分元素的相关信息,请回答相关问题。
(1)下列各组元素具有相似化学性质的是 。(填序号)
①He和Ar②He和Mg③Al和Si④F和Cl
(2)写出具有10个电子的原子、阳离子和分子的符号各一个:原子 ,阳离子 ,分子 。
(3)钠元素的原子序数为 ,画出它的原子结构示意图 。
钠原子和氯原子形成的化合物是由 (填“原子”“离子”“分子”)构成的。
在 100 g溶质的质量分数为5%的食盐溶液中加入5 g食盐再加100 g水,完全溶解后,溶液的质量为 ,溶质的质量为 ,溶质的质量分数为