常温下,向l00mL 0.01 mol•L-1盐酸中逐滴加入0.02 mol•L-1 MOH溶液,如下图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是( )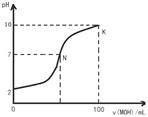
| A.MOH是弱碱 |
| B.N点c(Cl-) = c(M+) |
C.随着MOH溶液的滴加,比值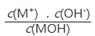 不变 不变 |
| D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol•L-1 |
下列褪色过程不是因为氧化还原反应而褪色的是()
| A.SO2气体通入溴水使溴水褪色 |
B.氯水使滴有酚酞的NaOH溶液褪色,加入N aOH后不变红 aOH后不变红 |
| C.将苯滴入溴水中振荡,溴水层褪色 |
| D.将含有碘单质的淀粉溶液,加入NaOH溶液后蓝色褪去 |
下列现象或事实可用同一化学原理加以说明的是()
| A.氯化铵和氯化钠的混合物、碘和氯化钠的混合物都可以用加热法进行提纯 |
| B.氯水和二氧化硫气体均能使品红溶液褪色 |
| C.硫酸亚铁溶液和氢氧化钠溶液在空气中久置后均会变质 |
| D.铁片和铝片置于冷的浓硫酸中均无明显现象 |
下列说法正确的是()
| A.IA族元素的金属性一定比IIA族元素的金属性强 |
| B.ⅥA族元素中氢化物最稳定的其沸点一定最高 |
C.非金属元素只能形 成共价化合物 成共价化合物 |
| D.短周期中,同周期元素的离子半径从左到右逐渐减小 |
“神州七号”三兄弟——LiH、LiD、LiT。其中Li的质量数为7,对这三种物质的下列说法正确的是()
A.质子数之比为1:2:3 B.中子数之比为1:1:1
C.摩尔质量之比为8:9:10 D.化学性质不相同
在25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na 2CO3溶液中,下列判断正确的是
| A.c(OH-)前者大于后者 | B.均存在电离平衡和水解平衡 |
| C.存在的粒子种类相同 | D.溶液中阳离子浓度相同 |