XeF4在水中的反应为:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。下列说法中正确的是
| A.XeF4分子中各原子均达到8电子稳定结构 |
| B.XeF4分子中Xe的化合价为0价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2∶3 |
| D.XeF4按上述方式水解,每生成4molXe,转移16mol电子 |
下列电子式中错误的是
| A.Na+ | B.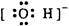 |
C.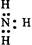 |
D. |
下列方法中,可用于除去小苏打溶液中混有的Na2CO3,最适宜的物质是
| A.氢氧化钙 | B.通入CO2 | C.碳酸氢钙 | D.加入盐酸 |
高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列说法正确的是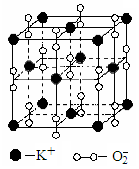
| A.超氧化钾的化学式为KO2,每晶胞含有4个K+和8个O2- |
| B.晶体中每个K+周围有8个O2-,每个O2-周围有8个K+ |
| C.晶体中与每个K+距离最近的K+有8个 |
| D.晶体中,0价氧原子与-2价氧原子的数目比为3:1 |
已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1 mol·L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中正确的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
D.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等
曲酸是一种非常有潜力的食品添加剂。经测定曲酸的分子式为C6H6O4,结构式如右图所示,试根据曲酸分子结构特点,推测曲酸不可能具有的性质为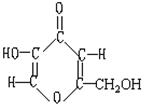
| A.能发生酯化反应 | B.易溶于水、醇 |
| C.具有抗氧化性 | D.具有强酸性 |