已知下列热化学方程式:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
Fe2O3(s)+ 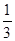 CO(g)
CO(g)
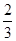 Fe3O4(s)+
Fe3O4(s)+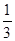 CO2(g);△H="-15.73" kJ/mol
CO2(g);△H="-15.73" kJ/mol
Fe3O4(s)+ CO(g) 3FeO(s)+CO2(g);△H="+640.4" kJ/mol
3FeO(s)+CO2(g);△H="+640.4" kJ/mol
则14 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为 ( )
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
NA代表阿伏加德罗常数,下列判断正确的是()
A.2.4g金属Mg变为Mg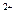 时失去的电子数为0.1 NA 时失去的电子数为0.1 NA |
| B.等物质的量的N2和CO所含原子数相同,质量相同 |
| C.在标况下,22.4 L H2O所含氢原子为2NA |
D.1L 0.1 mol·L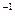 的乙酸溶液中H 的乙酸溶液中H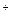 数为0.1 NA 数为0.1 NA |
下列离子方程式正确的是()
A.向盐酸中滴加氨水:H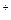 +OH +OH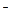 ==H2O ==H2O |
| B.向次氯酸钙溶液中通入少量的CO2: Ca 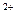 +2ClO +2ClO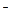 +H2O+CO2 ="==" CaCO3 +H2O+CO2 ="==" CaCO3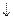 +2HClO +2HClO |
| C.将少量Cl2通入KBr、KI的混合溶液中 Cl2+2Br 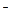 ==Br2+2Cl ==Br2+2Cl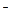 |
D.利用腐蚀法制作印刷线路板:Fe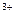 +Cu==Fe +Cu==Fe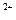 +Cu +Cu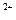 |
下列类型的反应,一定发生电子转移的是()
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
下列叙述正确的是()
| A.SO2具有还原性,故可作漂白剂 |
| B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C.浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| D.CaCO3在水中的溶解度很小,故CaCO3为弱电解质 |
能实现下列物质间直接转化的元素是()
单质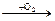 氧化物
氧化物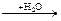 酸或碱
酸或碱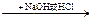 盐
盐
| A.硅 | B.硫 | C.铜 | D.铁 |