下列各组顺序的排列不正确的是( )
| A.原子半径:Na>Mg>Al>H | B.热稳定性: HC l<H2S<PH3 |
| C.酸性强弱:H2SiO3<H2CO3<H3PO4 | D.氧化性:K+<Na+<Mg2+<Al3+ |
250C,向1 mL pH=a的盐酸 中滴加10 mL pH=b的NaOH溶液,当溶液中
中滴加10 mL pH=b的NaOH溶液,当溶液中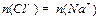 时,a+b的值为( )
时,a+b的值为( )
| A.13 | B.14 | C.15 | D.不能确定 |
在一密闭容器中充入1 mol CO和1 mol H2O(g),一定条件下反应: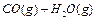
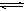
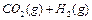 达到平衡时生成0.67mol CO
达到平衡时生成0.67mol CO 2,若在相同条件下将H2O(g)改为4mol,反应达到平衡时生成CO2的物质的量为( )
2,若在相同条件下将H2O(g)改为4mol,反应达到平衡时生成CO2的物质的量为( )
| A.1.34mol | B.1.0mol | C.0.94mol | D.0.52mol |
把Ca(OH)2放入蒸馏水中,一段时间后达到如下平衡: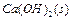
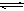
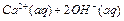 ,下列说法确的是( )
,下列说法确的是( )
| A.恒温下向溶液中加CaO,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
D.向溶液中加入少量NaOH固体,Ca(OH)2固体 质量不变 质量不变 |
弱电解质的电离程度可用电离度( )表示:
)表示: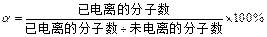 ,现有pH均为4的HCl和
,现有pH均为4的HCl和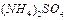 溶液,则两种溶液中H2O的电离度之比为( )
溶液,则两种溶液中H2O的电离度之比为( )
| A.1:2 | B.2:5 | C.1:106 | D.106:1 |
下列各式中属盐的水解反应的是( )
A.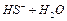 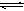 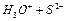 |
B.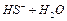 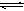 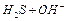 |
C.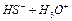 = =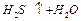 |
D.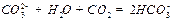 |